Ketone органдарынын Multi-өлчөмдүү ролдору
Кетон денелери боор тарабынан түзүлөт жана глюкоза адамдын организминде жеткиликтүү болбогондо энергия булагы катары колдонулат. Эки негизги кетон органы acetoacetate (AcAc) жана 3-бета-гидроксибутират (3HB), ацетон үчүнчү жана эң аз көп кетон денеси болуп саналат. Кетондор дайыма канда болот жана алардын деңгээли орозо кармоодо жана узакка созулган машыгууда жогорулайт.�гликогенолиз, организмдер май кислоталарынын жана кетогенетикалык амино-кислотадан ажырашынан аркылуу ketone органдарды чыгара турган биохимиялык жараян.
Ketone органдар, негизинен, иштелип жатат Боор клеткаларынын митохондрия. Гликогенолиз, каны аз глюкоза бөлүмдөр бар болгондо келип чыгат, атап айтканда, мындай гликоген башка уюлдук карбонгидрат дүкөндөр, кийин, бүтүп калган. инсулин жетиштүү суммасы жок болсо, бул механизм да пайда болушу мүмкүн. ketone органдарынын өндүрүш акыры май кислоталары адамдын денесинде сакталат жеткиликтүү энергия үчүн козголгон. Гликогенолиз, ал өз алдынча жөнгө салынат митохондрия болот.
жалпылаган
Ketone орган зат психологиялык гомеостаз борбордук түйүн болуп эсептелет. Бул карап, биз кетондор азык калдыктары түрдүү органдарды жана организм оптималдаштыруу жана бир нече органдар системаларынын сезгенүүсүнүн жана жаракат коргоо дискреттик жакшы-тюнинг зат ролдорун кызмат болору талкууланат. карбонгидрат көп болгондо Адатта зат субстраттардын карбонгидрат чектөө гана аталган катары каралып, акыркы байкоолор ketone органдарынын маанилүү эле маанилүү зат экенин жана медиаторлор билдиребиз. толкунданып системасынын оорулары белгилүү дарылоо жолдору бир репертуарына толуктоо, рак менен ketone органдарынын келечектүү ролдор семирүү байланыштуу жана жүрөк-кан тамыр оорулары менен дарылоо ыкмаларын ачып, жүрөк, боор менен кызыктуу коргоо милдеттери бар сыяктуу эле, келип чыккан. ketone зат жана сигналдаштыруунун менен байланыштуу заманбап байкоо менен классикалык окуулар менен элдештирүү үчүн талкууланат.
тааныштыруу
Кетон денелери жашоонун бардык чөйрөлөрү, эукария, бактериялар жана археялар үчүн маанилүү альтернативалуу метаболикалык отун булагы болуп саналат (Aneja et al., 2002; Cahill GF Jr, 2006; Krishnakumar et al., 2008). Адамдардагы кетон денесинин метаболизми аш болумдуу заттардын жетишсиздигинен эпизоддук мезгилде мээни күйгүзүү үчүн пайдаланылган. Кетон денелери сүт эмүүчүлөрдүн ?-кычкылдануу (ФАО), трикарбон кислотасынын цикли (TCA), глюконеогенез, де-ново липогенез (DNL) жана стеролдордун биосинтези сыяктуу маанилүү метаболизм жолдору менен чырмалышкан. Сүт эмүүчүлөрдө кетон денелери негизинен боордо ФАОдон алынган ацетил-КоАдан өндүрүлөт жана алар терминалдык кычкылдануу үчүн боордон тышкары ткандарга ташылат. Бул физиология май кислотасынын болушун көбөйтүп, карбонгидраттын болушун азайтуучу орозо кармоонун салыштырмалуу кыска мөөнөттөрү менен көбөйтүлгөн альтернативалуу отун менен камсыз кылат (Cahill GF Jr, 2006; McGarry and Foster, 1980; Robinson and Williamson, 1980). Кетондун денесинин кычкылдануусу көптөгөн физиологиялык абалдарда, анын ичинде орозо, ачкачылык, неонаталдык мезгил, көнүгүүдөн кийинки, кош бойлуулук жана карбонгидраттуу диетаны кармануу сыяктуу көптөгөн физиологиялык абалдарда боордон тышкары ткандардын ичиндеги жалпы энергетикалык сүт эмүүчүлөрдүн метаболизмине олуттуу салым кошот. Дени сак бойго жеткен адамдарда кетондун жалпы концентрациясы циркадиялык термелүүлөрдү адатта болжол менен 100-250 μM көрсөтөт, узакка созулган көнүгүүдөн же 1 сааттык орозодон кийин ~ 24 мМге чейин көтөрүлөт жана диабеттик кетоацидоз сыяктуу патологиялык абалда 20 мМге чейин чогулат. Cahill GF Jr, 2006; Johnson et al., 1969b; Koeslag et al., 1980; Robinson and Williamson, 1980; Wildenhoff et al., 1974). Адамдын боору суткасына 300 г кетон денесин өндүрөт (Balasse and Fery, 1989), алар тамактанган, ачка калган жана ачка калган учурларда жалпы энергия чыгымынын 5-20% түзөт (Balasse et al., 1978; Cox et al., 2016). ал., XNUMX).
Акыркы изилдөөлөр азыр сүт эмүүчүлөрдүн клетка зат ketone органдарынын маанилүү ролун баса, гомеостаз жана психологиялык жана патологиялык мамлекеттердин ар кандай астында сигналдаштыруунун. Мындан тышкары, мээ, жүрөк, же таргыл болуп extrahepatic кыртыштарга энергетикалык күйүүчү кызмат кылып, ketone органдары белги ортомчу катары маанилүү ролду ойнойт, белок пост-котормочулук өзгөртүүлөрдү (PTM) айдоочулары, сезгенүү жана кычкылданууга стресске медиаторлорго. Бул карап, биз ketone органдардын жана алардын зат pleiotropic ролдору классикалык жана азыркы көз карашын камсыз кылат.
Ketone Body зат баяндама
Боордун кетогенезинин ылдамдыгы майдын физиологиялык жана биохимиялык кайра түзүлүшү менен жөнгө салынат. Негизги жөнгө салуучуларга триацилглицеролдордон май кислоталарынын липолизи, гепатоциттердин плазма мембранасы аркылуу жана аркылуу ташуу, карнитин пальмитойлтрансфераза 1 (CPT1) аркылуу митохондрияга ташуу, ?-кычкылдануу спиралы, TCA циклинин активдүүлүгү жана аралык концентрациялар, редоксалдык потенциалдар, гормоналдык потенциалдар жана реоксульаторлор кирет. бул процесстердин, негизинен глюкагон жана инсулин [каралып чыккан (Arias ж.б., 1995; Айте ж.б., 1993; Ehara ж.б., 2015; Ferre ж.б., 1983; Кан ж.б., 2005; МакГарри жана Фостер. , 1980; Williamson et al., 1969)]. Классикалык түрдө кетогенез агып чыгуу жолу катары каралат, мында ?-кычкылдануудан алынган ацетил-КоА цитрат синтаза активдүүлүгүнөн жана/же оксалоацетаттын цитраттын пайда болушу үчүн конденсациядан ашат. Үч көмүртектүү аралык заттар, кыязы, ацетил-КоА керектөө үчүн оксалоацетат бассейнин кеңейтүү жөндөмдүүлүгүнө байланыштуу анти-кетогендик активдүүлүктү көрсөтөт, бирок боордогу ацетил-КоА концентрациясы гана кетогендик ылдамдыкты аныктабайт (Foster, 1967; Rawat and Menahan, 1975; Williamson ж.б., 1969). Кетогенезди гормоналдык, транскрипциялык жана пост-трансляциялык окуялар менен жөнгө салуу кетогендик ылдамдыкты так жөнгө салуучу молекулярдык механизмдер толук түшүнүлө элек деген түшүнүктү колдойт (HMGCS2 жана SCOT/OXCT1 жобосун караңыз).
Кетогенез негизинен боордун митохондриялык матрицасында майдын жалпы кычкылданышына пропорционалдуу ылдамдыкта болот. Ацил чынжырлары митохондриялык мембраналар аркылуу жана ?-кычкылдануу аркылуу өткөндөн кийин, 3-гидроксиметилглутарил-КоА синтазасынын (HMGCS2) митохондриялык изоформасы ацетоацетил-КоА (AcAc-CoA) конденсацияланышын жана H-AM генерациясын ишке ашырган тагдырды катализдейт. (1А-сүрөт). HMG-CoA лиазасы (HMGCL) ацетил-КоА менен ацетоацетатты (AcAc) бөлүп чыгаруу үчүн HMG-CoAди ажыратат, ал эми экинчиси фосфатидилхолинге көз каранды митохондриялык дегидрогеназа (D-OHB) тарабынан d-?-гидроксибутиратка (d-?OHB) чейин төмөндөйт. BDH1) NAD+/NADH менен байланышкан тең салмактуулукка жакын реакцияда (Bock and Fleischer, 1975; LEHNINGER et al., 1960). BDH1 тең салмактуулуктун туруктуулугу d-?OHB өндүрүшүн жакшыртат, бирок AcAc/d-?OHB кетон денелеринин катышы митохондриялык NAD+/NADH катышына түз пропорционалдуу, ошондуктан BDH1 оксидоредуктаза активдүүлүгү митохондриялык редокс потенциалын модуляциялайт (Krebs et al., 1969; Williamson et al., 1967). AcAc ошондой эле кетоацидоз менен ооруган адамдарда таттуу жыттын булагы болгон ацетонго (Педерсен, 1929) өзүнөн-өзү декарбоксилдениши мүмкүн (б.а. жалпы кан сары суусунун кетон денелери > ~7 мМ; AcAc pKa 3.6, ?OHB pKa 4.7). Кетон денелери митохондриянын ички мембранасы аркылуу ташылуучу механизмдер белгисиз, бирок AcAc/d-?OHB клеткалардан монокарбоксилат ташыгычтар аркылуу чыгарылат (сүт эмүүчүлөрдө, MCT 1 жана 2, ошондой эле эриген затты ташуучу 16A үй-бүлө мүчөлөрү 1 жана 7) жана терминалдык кычкылдануу үчүн боордон тышкары ткандарга айланууда ташылат (Cotter et al., 2011; Halestrap and Wilson, 2012; Halestrap, 2012; Hugo et al., 2012). Айлануучу кетон денелеринин концентрациясы боордон тышкаркы кыртыштарга караганда жогору (Харрисон жана Лонг, 1940) кетон телолору концентрация градиенти боюнча ташылып жатканын көрсөтөт. MCT1деги функцияны жоготуу мутациялары кетоацидоздун өзүнөн-өзү пайда болушу менен байланышкан, бул кетондун денесин импорттоодо маанилүү ролду сунуштайт.
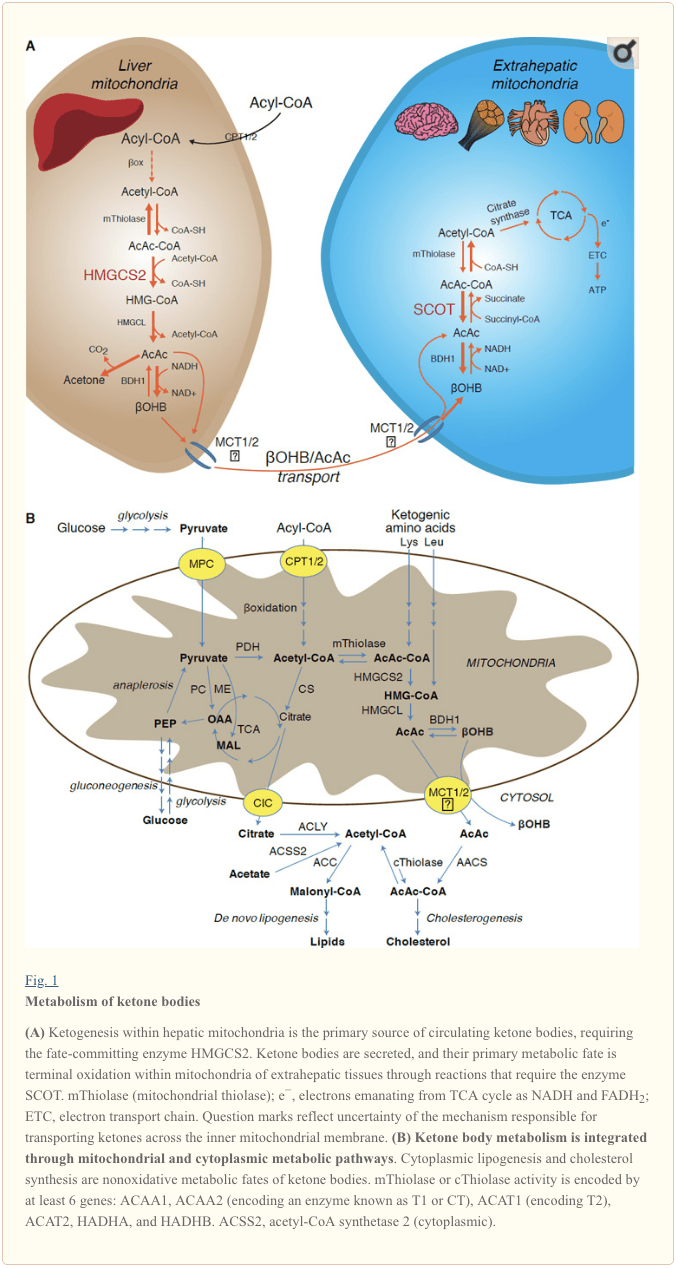
Кетон денелеринин кычкылданбаган тагдырларга потенциалдуу бурулуп кетишин кошпогондо (к. Кетон денелеринин кычкылданбаган метаболизмдик тагдыры), гепатоциттерде алар чыгарган кетон денелерин метаболизмге алуу жөндөмү жок. Боор тарабынан де-ново синтезделген кетон денелери (i) боордон тышкары ткандардын митохондрияларында ацетил-КоАга катаболизацияланат, ал терминалдык кычкылдануу үчүн TCA циклинде жеткиликтүү (1А-сүрөт), (ii) липогенезге же стерол синтезинин жолдоруна бурулат. Сүрөт 1B), же (iii) заара менен бөлүнүп чыгат. Альтернативдик энергетикалык отун катары кетон денелери жүрөктө, скелет булчуңунда жана мээде катуу кычкылданат (Balasse and Fery, 1989; Bentourkia et al., 2009; Owen et al., 1967; Reichard et al., 1974; Sultan, 1988). ). Боордон тышкаркы митохондриялык BDH1 OHB кычкылдануусунун биринчи реакциясын катализдеп, аны кайра AcAcге айландырат (LEHNINGER ж.б., 1960; Sandermann ж.б., 1986). Цитоплазмалык d-?OHB-дегидрогеназа (BDH2) BDH20ге болгону 1% ырааттуулугу менен кетон денелери үчүн жогорку Кмге ээ, ошондой эле темир гомеостазында роль ойнойт (Davuluri et al., 2016; Guo et al., 2006) . Боордон тышкаркы митохондриялык матрицада AcAc сүт эмүүчүлөрдүн уникалдуу КоА трансферазасы, сукцинил-КоА:3-оксокислота-КоА трансферазасы (SCOT, CoA трансфераза) менен катализделген реакцияда сукцинил-КоАдан КоА-бөлүкчөсүн алмашуу аркылуу AcAc-CoAга активдештирилет; OXCT1 тарабынан коддолгон), жакын тең салмактуулук реакциясы аркылуу. AcAc-CoA гидролизинде бөлүнүп чыккан бош энергия сукцинил-КоАга караганда көбүрөөк, бул AcAc пайда болушуна шарт түзөт. Ошентип, кетон денесинин кычкылдануу агымы массалык аракеттен улам пайда болот: AcAc мол запасы жана цитрат синтаза аркылуу ацетил-КоА тез керектөө SCOT тарабынан AcAc-CoA (+ сукцинат) пайда болушуна шарт түзөт. Белгилеп кетсек, глюкозадан (гексокиназа) жана май кислоталарынан (ацил-КоА синтетазаларынан) айырмаланып, кетон денелеринин (SCOT) кычкылдануучу формага активдешүүсү АТФтин инвестициясын талап кылбайт. Кайтарылуучу AcAc-CoA тиолаза реакциясы [ACAA2 (T1 же CT деп аталган ферментти коддоочу), ACAT1 (коддоочу T2), HADHA же HADHB менен коддолгон төрт митохондриялык тиолазанын кайсынысы менен катализделген] ацетил-КоАнын эки молекуласын берет, TCA циклине кирет (Hersh and Jencks, 1967; Stern et al., 1956; Williamson et al., 1971). Кетотикалык абалдарда (б.а. жалпы сарысудагы кетондор > 500 μM), кетон денелери энергияны сарптоого олуттуу салым кошот жана кычкылдануу же каныкканга чейин ткандарда тез колдонулат (Balasse et al., 1978; Balasse and Fery, 1989). Edmond et al., 1987). Боордон алынган кетон денелеринин өтө аз бөлүгүн заарада оңой өлчөөгө болот, ал эми бөйрөктүн колдонуу жана реабсорбция ылдамдыгы айлануудагы концентрацияга пропорционалдуу (Goldstein, 1987; Robinson and Williamson, 1980). Жогорку кетотикалык абалдарда (плазмада> 1 мМ), кетонурия кетоздун жарым-сандык кабарчысы катары кызмат кылат, бирок заара кетон денелеринин көпчүлүк клиникалык анализдери AcAcти аныктайт, бирок ?OHB эмес (Klocker et al., 2013).
Кетогенетикалык субстраттардын жана Hepatocyte зат алардын таасири
Кетогенетикалык субстраттардын май кислоталарын турган амино-кислоталарды клетканын (сүрөт. 1B) кирет. айрыкча, орнитин, амино-кислотадан катаболизм, пост-absorptive мамлекеттик ketone органдарынын тууралуу 4% түзөт (Thomas .Удаалаш., 1982). Ошентип, анткени ролунун карбонгидрат менен камсыз кылуу учурунда, негизинен, май кислоталарынын чыккан ketone органдарын түзүү үчүн acetyl-КоА-субстрат бассейн, кайра карату негизинен anaplerosis аркылуу боор Баракелде айлампасын кирет, башкача айтканда, ATP көз каранды carboxylation oxaloacetate үчүн (апр), же Картошка менен (MAL) эмес, кычкылдануу decarboxylation acetyl-КоА үчүн (Jeoung ж.б., 2012. Магнуссон ж.б., 1991. Мерритт, ж.б. 2011.). боордо, глюкоза жана кайра карату гана өлчөмдө (Jeoung ж.б.., 2012) acetyl-КоА-максималдуу болуп кайра карату да decarboxylation, гликогенолиз, өбөлгө түзөт.
Acetyl-КоА-терминалдык кычкылданууга аркылуу ATP муунга тышкары боор ортомчулук зат (ошондой эле ketone орган метаболизм, пост-котормочулук өзгөртүүлөрдү жана клетка дене бир бүтүндүктө карагыла) ажырагыс бир нече ролдорду камтып. Acetyl-КоА-ГТС кыймылга (i) кайра карату карбоксилаз (ЭЭМ), ошону менен anaplerotic Баракелде айлампасынын салып метаболиттерди кирүүсүнө өрчүндөйт бир зат башкаруу механизмин иштетип (Оуэн, ж.б. 2002. Scrutton жана сырткы, 1967) жана (ii) кайра карату dehydrogenase phosphorylates жана кайра карату dehydrogenase (PDH) тоскоол Креатинкиназа, (Купер .Удаалаш., 1975), ошону менен бирге андан ары anaplerosis аркылуу Баракелде айлампасынын салып кайра карату агымын жогорулатуу. Мындан тышкары, cytoplasmic acetyl-КоА, анын бассейн метаболиттер ташуу үчүн митохондриялык acetyl-КоА-кайра механизмдер менен толукталган, май кислотасы кычкылдатууну коркот: acetyl-КоА-карбоксилаз (КБА) malonyl-КоА, lipogenic субстрат менен acetyl-КоА Кудайга кайрылганы көмөктөшөт жана митохондриялык CPT1 менен аллостерикалык ингибиторун [каралганда (Кан .Удаалаш, 2005. МакГарри жана багып, 1980)]. Ошентип, митохондриялык acetyl-КоА-эки жөнгө топтоо менен боор ортомчулук зат негизги жактарын ланыштын гликогенолиз, ишке өтүүсүнө жолуна менен жөнгө салынат.
Ketone органдарынын келишимдик кычкылданууга метаболизма тагдырлары
боор-алынган кетондор басымдуу тагдыры Scot көз каранды extrahepatic кычкылдануу болуп саналат. Бирок, Acac cytoplasmic acetoacetyl-КоА-синтетаз (AACS, сүрөт. 1B) тарабынан кылдат ылгоодон Acac-КоА тарабынан ATP көз каранды чыгууларга кайрылуу аркылуу анаболикалык жолунан митохондрия жана пайдалануу экспорттоого болот. Бул жолду мээ иштеп чыгуу учурунда жана Желин баштыкчасы эмизген жигердүү эмес (Morris, 2005; Робинсон жана Мукасан, 1978; Ohgami ж.б., 2003.). AACS да жогорку кемик көрсөтүлөт жана osteoclasts ишке (Aguilo .Удаалаш, 2010.. Yamasaki, ж.б. 2016). Cytoplasmic Acac-КоА-да cytosolic HMGCS1 sterol биосинтези көздөй, же-КоА-acetyl эки cytoplasmic thiolases биринин жабышып (ACAA1 жана ACAT2) тарабынан багытталган, malonyl-КоА үчүн carboxylated, жана май кислоталарынын (Bergstrom ет синтездөөгө өбөлгө болот Сүрөсү, 1984. Эдмонд, 1974; Endemann ж.б., 1982.. инетке ж.б., 1983; Webber жана Эдмонд, 1977).
Физиологиялык мааниси али аныктала элек болсо да, кетондор боордо да анаболикалык субстрат катары кызмат кыла алат. Жасалма эксперименталдык контексттерде AcAc жаңы синтезделген липиддердин жарымына жана жаңы синтезделген холестеролдун 75% га чейин салым кошо алат (Endemann et al., 1982; Geelen et al., 1983; Freed et al., 1988). AcAc боор майынын толук эмес кычкылдануусунан алынгандыктан, AcAcтин in vivo липогенезге салым кошуу жөндөмдүүлүгү боордун пайдасыз циклин билдирет, мында майдан алынган кетондор липиддерди өндүрүү үчүн колдонулушу мүмкүн, бул түшүнүк физиологиялык мааниси эксперименталдык текшерүүнү талап кылат, бирок бул түшүнүк. адаптивдүү же адаптивдик ролдор (Solinas et al., 2015). AcAc аз AACS Km-AcAc (~ 50 μM) менен холестерогенезди ынтызарлык менен камсыздайт, ал тургай тамактанган абалда да AcAc активдештирүүгө жардам берет (Бергстром ж.б., 1984). Цитоплазмадагы кетон метаболизминин динамикалык ролу чычкандын алгачкы эмбриондук нейрондорунда жана 3T3-L1 туунду-адипоциттерде сунушталган, анткени AACS кулатуусу ар бир клетка түрүнүн дифференциациясын начарлатты (Hasegawa et al., 2012a; Hasegawa et al., 2012b). In vivo чычкандарда AACS кулатуусу кан сары суудагы холестеролду азайткан (Hasegawa et al., 2012c). SREBP-2, холестерол биосинтезинин башкы транскрипциялык жөнгө салуучусу жана пероксисома пролифератору активдештирилген рецептор (PPAR)-? AACS транскрипция активаторлору болуп саналат жана нейриттин өнүгүүсүндө жана боордо анын транскрипциясын жөнгө салат (Aguilo et al., 2010; Hasegawa et al., 2012c). Чогуу алганда, цитоплазмалык кетон денесинин метаболизми тандалган шарттарда же оорунун табигый тарыхында маанилүү болушу мүмкүн, бирок боордон келип чыккан кетон денелерин жок кылуу үчүн жетишсиз, анткени массалык гиперкетонемия функциянын мутацияларын жоготуу аркылуу негизги кычкылдануучу тагдырдын тандалма бузулушунун шартында пайда болот. SCOT (Berry et al., 2001; Cotter et al., 2011).
HMGCS2 жана бодибилдинг / OXCT1 жөнгө салуу
улам, дене салмагын өлчөмдө жогорку мээ менен түрлөрдүн боор гликогенолиз, колдоо зарылчылыгы ген коддоо cytosolic HMGCS бир митохондриялык айырмачылыктары эрте омурткалуу өзүнөн болгон (Boukaftane .Удаалаш, 1994. Cunnane жана Crawford, 2003). Табигый түрдө пайда болгон жоготуу-жылдын иштеп HMGCS2 адамдардын геномдук hypoketotic гипогликемия башаламандыктарды алып (Питт, ж.б. 2015. Томпсон, ж.б. 1997.). Robust HMGCS2 сөз hepatocytes жана Colonic эпителий, анын сөз жана иш-аракет Enzymatic ар кандай механизмдер аркылуу макулдашылат менен чектелген (Mascaró .Удаалаш, 1995. МакГарри жана багып, 1980; Робинсон жана Мукасан, 1980). HMGCS2 таасир психологиялык мамлекеттердин толук көлөмү андан ары баштарынан талап кылат, ал эми анын сөздөр жана / же ишин эрте төрөттөн мезгил, карылыктан, кант диабети, кетогенетикалык диета (Balasse жана Fery ачарчылыктан же Жута, 1989 ичинде жөнгө салынат; Кехилл ГК JR, 2006 ; Джирард ж.б., 1992. Hegardt, 1999; Satapati ж.б., 2012.. азгырма, ж.б., 2010). Түйүлдүктө Hmgcs5 генинин 2-кабаттуу аймагынын метилдениши анын транскрипциясы менен тескери корреляцияланат жана төрөлгөндөн кийин жарым-жартылай тескери болот (Arias et al., 1995; Ayte et al., 1993; Ehara et al., 2015; Ferre et al. ., 1983). Ошо сыяктуу эле, боор Bdh1 отъема туулган өсүп, бир өнүгүү көрсөткөн үлгү көрсөткөн, ошондой эле fibroblast өсүшү себеп (ёёёёё) -21 көз каранды абалда болгон кетогенетикалык диета менен азгырган (Badman .Удаалаш, 2007 жатат.. Чжан, ж.б. 1989 ). сүт эмүүчү гликогенолиз, инсулин жана глюкагон да өтө сезимтал болуп, тыюу жана стимулданышы, тиешелүүлүгүнө жараша (МакГарри жана багып, 1977). Инсулин глюкагон боордо (Hegardt, 1999) түздөн-түз таасир аркылуу кетогенетикалык къаны жогорулатат, ал эми, бул анын субстрат менен гликогенолиз, ажыратуу, кемик ткань lipolysis бөгөт коюуда. Hmgcs2 копиялоо forkhead жүргүзүлсө протоколдун себеби FOXA2, инсулин-phosphatidylinositol-3-Креатинкиназа аркылуу тосулуп жатат / AKT жана глюкагон-Camp-p300 белги (Ариас .Удаалаш менен башчыны да ынандырууга болот стимулданганда, 1995. Hegardt, 1999; Былтыр декабрда ж.б.. , 1990; Thumelin ж.б., 1993. из Meyenn ж.б., 2013.. Wolfrum ж.б., 2004; Wolfrum ж.б., 2003).. PPAR? (Родригес ж.б., 1994) анын максаты менен бирге, FGF21 (Бадман ж.б., 2007) ошондой эле ачкачылык же кетогендик диетаны башкаруу учурунда боордо Hmgcs2 транскрипциясын жаратат (Badman et al., 2007; Inagaki et al., 2007). ). PPAR индукциясы? түйүлдүктөн неонаталдык физиологияга өткөнгө чейин пайда болушу мүмкүн, ал эми FGF21 активдешүү гистон деацетилазасынын (HDAC) -3 (Rando et al., 2016). mTORC1 (rapamycin комплексинин сүт эмүүчүлөрдүн максаттуу 1) PPAR көз каранды бөгөт коюу? транскрипциялык активдүүлүк ошондой эле Hmgcs2 генинин экспрессиясынын негизги жөнгө салуучусу (Sengupta ж.б., 2010) жана боор PER2, мастер циркадиялык осциллятор, Hmgcs2 экспрессиясын кыйыр түрдө жөнгө салат (Chavan et al., 2016). Акыркы байкоолор боордон тышкаркы шишик менен шартталган интерлейкин-6 PPAR аркылуу кетогенезди бузат экенин көрсөтүп турат? басуу (Flint et al., 2016).
HMGCS2 энзимдин иш-аракет бир нече PTMs аркылуу жөнгө салынат. HMGCS2 серин phosphorylation экстракорпоралдык өз ишин күчөтүлгөн (Grimsrud ж.б.., 2012). HMGCS2 иши ГТС succinyl-КоА жана метионин калган succinylation (Ариас .Удаалаш тарабынан тосулуп турат, 1995. Hegardt, 1999; Лоудун жана Tubbs, 1985; Былтыр декабрда, ж.б. 1990. Rardin ж.б., 2013. Рид, ж.б.. 1975. Thumelin ж.б., 1993). HMGCS2 боюнча Succinylation, HMGCL, боор митохондрия Над + көз каранды deacylase sirtuin 1 (SIRT5) кабылышат жана BDH5 метионин калдыктары (Rardin ж.б.., 2013). HMGCS2 иши да SIRT3 метионин deacetylation жардам берет, ал acetylation жана succinylation ортосундагы Crosstalk HMGCS2 ишин (Rardin ж.б., 2013. Шимазу ж.б., 2013.) Жөнгө салат деп божомолдоого болот. HMGCS2 км Vmax жөнгө салуу ушул PTMs жөндөмдүүлүгүнө карабастан, бул PTMs курсу ге кылдат картага жана эмес, бододо, гликогенолиз, жана механикалык айдоочу болуп тастыкталган жок.
Scot hepatocytes да башка, митохондрияны тепсеген бардык сүт эмүүчүлөрдүн клеткалар менен көрсөтүлөт. Scot ишинин жана ketolysis мааниси улам 48h ичинде hyperketonemic гипогликемия төрөттөн кийинки бирдиктүү жоокер болду көргөзмөгө Scot-KO чычкандар, көрсөтүлгөн (Коттер ж.б.., 2011). нейрон же скелет myocytes жана бодибилдинг боюнча Tissue атайын жоготуу ачарчылыктан учурунда зат бузулууларды, бирок коркунуч туудурган эмес, алдыруучу (Коттер ж.б.., 2013b). адамдардын, бодибилдинг кемчилик башында катуу ketoacidosis менен өмүр, начарлыгын алып, кусуу жана комага (Берри менен ал берет, 2001.. Fukao ж.б., 2000. Kassovska-Bratinova ж.б., 1996; Niezen-Кинг ж.б.. , 1997; Saudubray ж.б., 1987.. Snyderman ж.б., 1998; Tildon жана Cornblath, 1972). Салыштырмалуу аз Scot гендик жана белок сөз жөнгө жөнүндө уюлдук деъгээлинде белгилүү. Oxct1 РНК сөз айкашы жана бодибилдинг белок жана иш ketotic мамлекеттер, сыягы, PPAR-каранды механизмдер (Fenselau жана Уоллис аркылуу азайып жатат, 1974; Fenselau жана Уоллис, 1976; Grinblat ж.б., 1986. Экибулак ж.б., 1991. Чолодо ж.б. ., 2001. Баста, ж.б. 2010). диабет ketoacidosis жылы боор гликогенолиз, жана extrahepatic кычкылданууга келбестиги Scot иш түшүүсүнүн менен ого бетер болот. cardiomyocytes менен инсулин-алдынча глюкоза ташуу (GLUT1 / SLC2A1) жөнүндө Overexpression да Oxct1 ген сөздөр жана кетондор эмес ketotic абалда терминалдык кычкылдатууну downregulates тоскоол (Ян ж.б.., 2009). боордо, Oxct1 РНК көп неонаталдык мезгилге түйүлдүктүн чейин microRNA-122 жана гистон methylation H3K27me3 өтүү учурунда көрүнүп турат тарабынан тыюу салынат (Thorrez .Удаалаш., 2011). Бирок, төрөгөндөн кийинки мезгилде боор Oxct1 сөз бөгөт боор эмес, айыккыс айырмачылыгына hepatocytes мурда иштеп жаткан Oxct1 сөз бир жоготуудан как тамыр аталары Oxct1-билдирүү бошотуусунан үчүн, биринчи кезекте, таандык болот. Чынында эле, ар hepatocytes жылы Oxct1 РНКнын Scot белок сөздөр өтө төмөн болуп саналат (Orii .Удаалаш., 2008).
SCOT ошондой эле PTMs тарабынан жөнгө салынат. Фермент SIRT3 KO чычкандарынын мээсинде гипер-ацетилденген, ал ошондой эле AcAc көз каранды ацетил-КоА өндүрүшүнүн төмөндөшүн көрсөтөт (Dittenhafer-Reed et al., 2015). SCOTтин тирозин калдыктарын ферментативдик эмес нитрлөө да анын активдүүлүгүн басаңдатат, бул ар кандай диабет чычкандарынын жүрөктөрүндө (Маркондес ж.б., 2001; Турко ж.б., 2001; Ванг ж.б., 2010a). Ал эми триптофан калдыктары нитрлөө SCOT активдүүлүгүн жогорулатат (Br�gère et al., 2010; Rebrin et al., 2007). SCOT активдүүлүгүн модуляциялоо үчүн иштелип чыккан калдык-спецификалык нитрлөө же де-нитрлөө молекулярдык механизмдери болушу мүмкүн жана түшүндүрүүнү талап кылат.
Extrahepatic гликогенолиз, ичинде талаш
Сүт эмүүчүлөрдүн негизги кетогендик органы боор болуп саналат жана гепатоциттер жана ичеги эпителий клеткалары гана HMGCS2нин митохондриялык изоформасын көп чагылдырышат (Cotter et al., 2013a; Cotter et al., 2014; McGarry and Foster, 1980; Robinson and Williamson, 1980) . Татаал полисахариддердин анаэробдук бактериялык ачытуусу бутиратты берет, аны сүт эмүүчүлөрдүн колоноциттери терминалдык кычкылдануу же кетогенез үчүн сиңирип алат (Cherbuy et al., 1995), ал колоноциттердин дифференциациясында роль ойношу мүмкүн (Wang et al., 2016). Ичеги эпителий клеткаларын жана гепатоциттерди кошпогондо, HMGCS2 башка сүт эмүүчүлөрдүн дээрлик бардык клеткаларында жок, бирок боордон тышкары кетогенездин келечеги шишик клеткаларында, борбордук нерв системасынын астроциттеринде, бөйрөктө, уйку безинде ? клеткалар, торчонун пигмент эпителийи (RPE), ал тургай скелет булчуңунда (Adijanto ж.б., 2014; Avogaro ж.б., 1992; El Azzouny ж.б., 2016; Grabacka ж.б., 2016; Канг ж. ; Le Foll et al., 2015; Nonaka et al., 2014; Takagi et al., 2016a; Thevenet et al., 2016; Zhang et al., 2016). Эктопиялык HMGCS2011 таза кетогендик кубаттуулугу жок кыртыштарда байкалган (Кук жана башкалар, 2; Вентц ж. , 2016; Kostiuk et al., 2010; Meertens et al., 2).
Кетон органдарын кычкылдандырган ар кандай боордон тышкары ткандардын HMGCS2 көз карандысыз механизмдери аркылуу кетон органдарын топтоо мүмкүнчүлүгү бар (сүрөт 2A). Бирок, кетон денелеринин туруктуу абалы кан айлануудагы концентрациядан ашкан эч кандай боордон тышкары кыртыш жок (Cotter et al., 2011; Cotter et al., 2013b; Harrison and Long, 1940), бул кетон денелери ылдый ташылат деп баса белгилейт. MCT1/2-каранды механизмдер аркылуу концентрация градиенти. Көрүнүп турган extrahepatic кетогенездин бир механизми чындыгында кетон кычкылдануусунун салыштырмалуу начарлашын чагылдырышы мүмкүн. Кошумча мүмкүн болгон түшүндүрмөлөр кетон дененин пайда болуу чөйрөсүнө кирет. Биринчиден, де-ново кетогенез тиолазанын жана SCOTтун кайтарымсыз ферменттик активдүүлүгү аркылуу пайда болушу мүмкүн (Weidemann and Krebs, 1969). Ацетил-КоА концентрациясы салыштырмалуу жогору болгондо, адатта AcAc кычкылдануусуна жооптуу реакциялар тескери багытта иштейт (GOLDMAN, 1954). Экинчи механизм ?-кычкылдануудан алынган аралык заттар TCA циклинин тар богоктугунан улам топтолгондо пайда болот, AcAc-CoA митохондриялык 3-гидроксиацил-КоА дегидрогеназа жана андан ары 3-гидроксибутирил менен катализделген реакция аркылуу l-?OHB-КоАга айландырылат. КоА деацилазадан l-?OHBге чейин, ал масс-спектрометрия же резонанстык спектроскопия менен d-?OHB физиологиялык энантиомеринен айырмаланбайт (Рид жана Озанд, 1980). l-?OHB хроматографиялык же энзимдик жактан d-?OHBден айырмаланышы мүмкүн жана боордон тышкары ткандарда бар, бирок боордо же канда жок (Hsu et al., 2011). Боор кетогенези BDH субстраты болгон жалгыз энантиомерди гана d-?OHB чыгарат (Ito et al., 1984; Lincoln et al., 1987; Reed and Ozand, 1980; Scofield et al., 1982; Scofield et al., 1982). 2). Үчүнчү HMGCS1990-көз карандысыз механизм d-?OHB аминокислота катаболизми аркылуу, атап айтканда лейцин менен лизинди жаратат. Төртүнчү механизм айкын көрүнүп турат, анткени ал маркерлөөчү артефактка байланыштуу жана псевдокетогенез деп аталат. Бул кубулуш SCOT жана тиолаза реакцияларынын кайтарымдуулугуна байланыштуу жана боордон тышкаркы ткандарда кетон денесинин тракеринин изотоптук суюлтуусунан улам кетон денесинин жүгүртүүсүн ашыкча баалоого алып келиши мүмкүн (Des Rosiers et al., 1988; Fink et al., 1990) . Ошого карабастан, псевдокетогенез көпчүлүк контексттерде анча деле маанилүү эмес болушу мүмкүн (Bailey et al., 1978; Keller et al., 2). Схема (сүрөт XNUMXA) кетондордун жогорулатылган кыртыштын туруктуу абалын эске алуу менен колдонууга пайдалуу мамилени көрсөтөт.
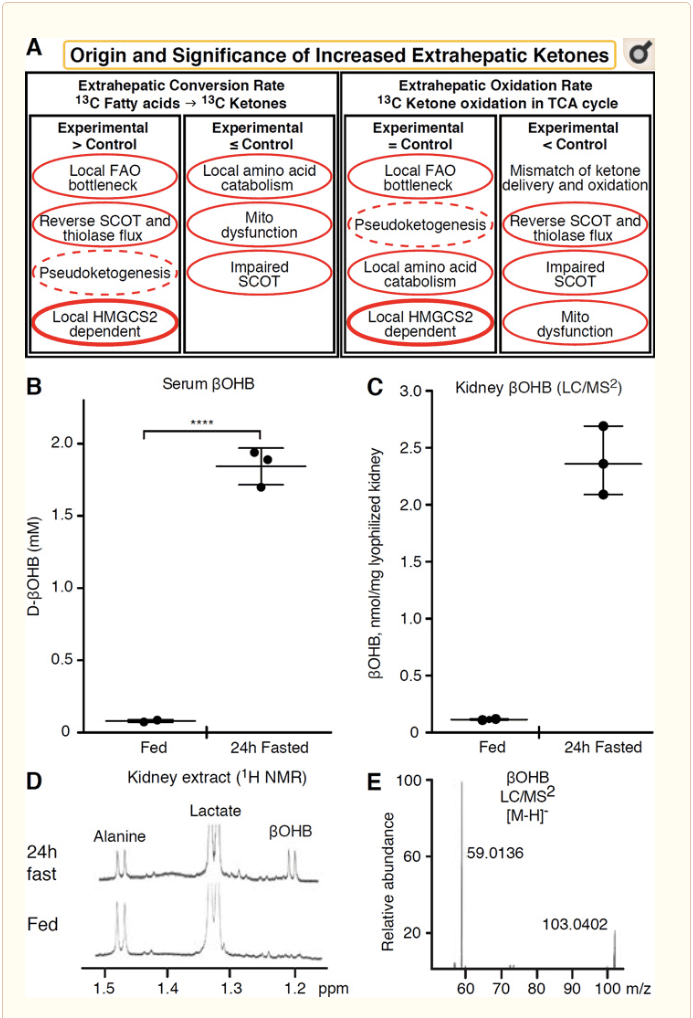

Жакында бөйрөк кетогендик орган катары көңүл бура баштады. Мамлекеттердин басымдуу көпчүлүгүндө бөйрөк боордон алынган кетон денелеринин таза керектөөчүсү болуп саналат, кетон денелерин кан агымынан бөлүп чыгарат же реабсорбциялайт, ал эми бөйрөк жалпысынан таза кетон денесинин генератору же концентратор эмес (Robinson and Williamson, 1980). Классикалык изилдөөнүн авторлору жасалма эксперименталдык системада сандык минималдуу бөйрөк кетогенези физиологиялык жактан тиешелүү эмес деген жыйынтыкка келишкен (Weidemann and Krebs, 1969). Жакында бөйрөк кетогенези диабетик жана аутофагия жетишсиз чычкан моделдеринде тыянак чыгарылды, бирок метаболикалык гомеостаздагы көп органдардын жылыштары бир нече органдарга киргизүү аркылуу интегративдик кетон метаболизмин өзгөртүшү ыктымал (Takagi et al., 2016a; Takagi et al., 2016b; Zhang et al., 2011). Акыркы басылмалардын бири бөйрөктүн кетогенезин бөйрөктөгү ишемия-реперфузиялык жаракаттан коргоочу механизм катары сунуш кылган (Tran et al., 2016). Чычкандардын бөйрөк кыртышынын экстракттарынан алынган ?OHB абсолюттук стабилдүү концентрациялары ~4�12 мМде билдирилди. Бул мүмкүн экенин текшерүү үчүн, биз тамактанган жана 24 саат ачкан чычкандардын бөйрөк экстракттарында ?OHB концентрациясын аныктадык. Сарысудагы OHB концентрациясы 100 сааттык орозодо ~2 μMден 24 ммге чейин жогорулады (2Б-сүрөт), ал эми бөйрөктөгү стабилдүү ?OHB концентрациясы тамактанган абалда болжол менен 100 μM, ал эми 1 саат ачка абалында болгону 24 мМ (сүрөт). 2C�E), 45 жыл мурун сандык концентрацияга шайкеш келген байкоолор (Хемс жана Броснан, 1970). Кетотикалык абалда боордон алынган кетон денелери ренопротектордук болушу мүмкүн, бирок бөйрөк кетогенезинин далилдери андан ары негиздөөнү талап кылат. Чыныгы боордон тышкары кетогенезди колдогон орчундуу далилдер RPEде берилген (Adijanto et al., 2014). Бул кызыктуу метаболизм трансформациясы RPEден алынган кетондордун фоторецепторлорго же Мюллер глия клеткаларына агып кетишине мүмкүндүк берүү үчүн сунушталган, бул фоторецептордун сырткы сегментинин регенерациясына жардам бере алат.
?OHB сигнал берүүчү ортомчу катары
Алар энергияга бай болгону менен, кетон денелери клеткалык гомеостазда провокациялык "канондук эмес" сигналдык ролду аткарышат (3-сүрөт) (Newman and Verdin, 2014; Rojas-Morales et al., 2016). Мисалы, ?OHB Гистондун acetylation көбөйтөт жана ошону менен кычкылдануу стрессти (Shimazu ж.б., 2013) кыскартуу гендердин экспрессиясын көбөйтөт класс I HDACs, бөгөт коюу. ?OHB өзү орозо кармаган же стрептозотоцин менен индукцияланган диабетик чычкандардын боорундагы лизин калдыктарында гистондун коваленттүү модификатору болуп саналат (Xie et al., 2016) (ошондой эле төмөндө караңыз, Кетон денесинин метаболизминин интеграциясы, трансляциядан кийинки модификациясы жана клетка физиологиясы, жана Кетон денелери, кычкылдануу стресстери жана нейропротекция).
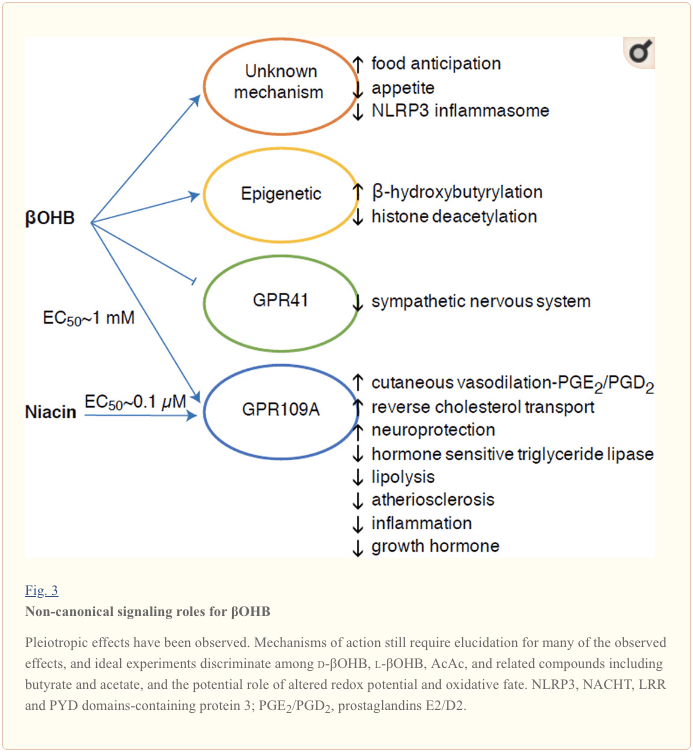
?OHB ошондой эле G-белок кошулган рецепторлор аркылуу эффектор болуп саналат. түшүнүксүз молекулярдык механизмдер аркылуу, ал симпатикалык толкунданып системасынын ишин басат жана G протеин кошулган кабылдагыч 41 (GPR41) аркылуу кыска чынжыр май кислотасынын сигналды бөгөт коюу менен жалпы энергия чыгымын жана жүрөктүн кагышын азайтат (Kimura et al., 2011). ?OHB эң көп изилденген сигналдык эффекттеринин бири GPR109A (ошондой эле HCAR2 катары белгилүү), майлуу ткандарда (ак жана күрөң) чагылдырылган гидрокарбон кислотасынын GPCR суб-үй-бүлө мүчөсү (Tunaru et al., 2003) аркылуу өтөт. иммундук клеткалар (Ahmed et al., 2009). ?OHB - d-?OHB, l-?OHB жана бутират тарабынан активдештирилген GPR109A рецепторунун (EC50 ~770 �M) жалгыз белгилүү эндогендик лиганды, бирок AcAc эмес (Taggart et al., 2005). GPR109A активдештирүү үчүн жогорку концентрация босогосуна кетогендик диетаны кармануу, ачарчылык же кетоацидоз учурунда жетишилет, бул май кыртышынын липолизинин бөгөт коюусуна алып келет. GPR109A антилиполитикалык таасири адениллил циклазанын жана cAMPтин төмөндөшү аркылуу ишке ашат, гормонго сезгич триглицерид липазасын тоскоол болот (Ahmed et al., 2009; Tunaru et al., 2003). Бул терс пикирлер циклин жаратат, анда кетоз кетогенезге модуляциялык тормозду орнотот, анда адипоциттерден этерификацияланбаган май кислоталарынын бөлүнүп чыгышын азайтат (Ахмед ж.б., 2009; Таггарт ж. липолизди стимулдайт симпатикалык диск. Ниацин (В2005 витамини, никотин кислотасы) GRP3A үчүн күчтүү (EC50 ~ 0.1 μM) лиганд болуп саналат, дислипидемияда ондогон жылдар бою эффективдүү колдонулат (Benyo et al., 109; Benyo et al., 2005; Fabbrini et al., a.;2006). Lukasova et al., 2010; Tunaru et al., 2011). Ниацин макрофагдарда тескери холестеролду ташууну жакшыртат жана атеросклеротикалык жараларды азайтат (Lukasova ж.б., 2003), ?OHB атеросклеротикалык жараларга тийгизген таасири белгисиз бойдон калууда. GPR2011A рецептору коргоочу ролду аткарса да, инсульт жана нейродегенеративдик ооруларда кетогендик диетаны колдонуунун ортосунда кызыктуу байланыштар бар (Fu et al., 109; Rahman et al., 2015), GPR2014A аркылуу ?OHBнин коргоочу ролу in vivo көрсөтүлгөн эмес. .
Акыр-аягы, ?OHB табитти жана токчулукка таасир этиши мүмкүн. Кетогендик жана өтө төмөн энергиялуу диеталардын таасирин өлчөгөн изилдөөлөрдүн мета-анализи, бул диетаны колдонгон катышуучулар контролдук диеталарга салыштырмалуу жогорку токчулукту көрсөтөт деген тыянакка келген (Gibson et al., 2015). Бирок, бул таасир үчүн акылга сыярлык түшүндүрмө табитти модуляциялоочу кошумча метаболизм же гормоналдык элементтер болуп саналат. Мисалы, кемирүүчүлөрдүн кетогендик диетасында сакталган чычкандар, ошондой эле калориялуулугуна карабастан, чуу контролу менен азыктанган чычкандарга салыштырмалуу энергия чыгымынын көбөйгөнүн көрсөтүштү жана айлануудагы лептин же тамактандыруунун жүрүм-турумун жөнгө салуучу пептиддердин гендери өзгөргөн жок (Кеннеди ж.б., 2007). ?OHB тарабынан табитти басууну сунуш кылган механизмдердин арасында сигнал жана кычкылдануу да кирет (Laeger et al., 2010). Циркадиандык ритм генинин (Per2) жана хроматиндин иммунопреципитациялык изилдөөлөрүнүн гепатоциттерге спецификалык делециясы PER2 түздөн-түз Cpt1a генин активдештирип, Hmgcs2ди кыйыр түрдө жөнгө салып, Per2 нокаут чычкандарында кетоздун бузулушуна алып келерин көрсөттү (Chavan et al., 2016). Бул чычкандар системалуу ?OHB башкаруу менен жарым-жартылай калыбына келтирилген бузулган тамак күтүү көрсөттү. Келечектеги изилдөөлөр түздөн-түз ?OHB максаттуу катары борбордук толкунданып системасын ырастоо үчүн керек болот, жана кетон кычкылдануу байкалган таасирлери үчүн талап кылынат, же башка сигнал механизми тартылган. Башка изилдөөчүлөр вентромедиалдык гипоталамустун ичинде жергиликтүү астроциттерден келип чыккан кетогенездин мүмкүнчүлүгүн тамак-ашты керектөөнүн жөнгө салуучусу катары чакырышкан, бирок бул алдын ала байкоолор генетикалык жана флюске негизделген баалоодон да пайда алып келет (Le Foll et al., 2014). Кетоз жана аш болумдуу заттардын жетишсиздигинин ортосундагы мамиле кызыкчылык бойдон калууда, анткени ачкачылык жана токчулук арыктоо аракетинде маанилүү элементтер болуп саналат.
Ketone Body метаболизм, Post-котормочулук өзгөртүүлөрдү жана клетка Physiology кошуу
Ketone органдары acetyl-КоА, уюлдук зат көрүнүктүү ролдорду көрсөтүүдө негизги аралык (Pietrocola ж.б.., 2015) жөнүндө compartmentalized көлмөлөргө өбөлгө түзөт. acetyl-КоА бири ролу acetylation үчүн субстрат болуп кызмат кылышы үчүн, ал бир enzymatically-кылдат ылгоодон гистон байланыштар өзгөртүү (Choudhary ж.б., 2014. Dutta ж.б., 2016. Fan ж.б., 2015.. Menzies ж.б., 2016 ). . Динамикалуу протеиндер эмес Enzymatic механизмдер аркылуу пайда болушу мүмкүн болгон көп acetylated бир топ, ошондой эле эсептөө Протеомика изилдөө (Dittenhafer-Камыш, ж.б. 2015 пайда болгон. Hebert ж.б., 2013; Rardin ж.б., 2013. ; Шимазу ж.б., 2010).. Метионин deacetylases бир цинк cofactor колдонуу (мисалы, nucleocytosolic HDACs) же NAD + чогуу субстрат (sirtuins, нежна) (Choudhary ж.б., 2014.. Menzies ж.б., 2016). acetylproteome бардык уюлдук acetyl-КоА-жылдын сенсор жана которо турган да катары кызмат көлмөгө, психологиялык жана генетикалык курал катары ар бир натыйжасы эмес Enzymatic дүйнөлүк acetylation өзгөртүлгөн (Weinert ж.б.., 2014). клеткадагы метаболиттерди метионин калган acetylation боюнча медиаторлорго катары кызмат кылып, Анын мол өтө динамикалуу ketone органдарынын ролун эске алуу маанилүү.
?OHB жок дегенде эки механизм аркылуу эпигенетикалык өзгөрткүч болуп саналат. Орозо кармоо, калорияны чектөө, түздөн-түз башкаруу же узакка созулган көнүгүү менен шартталган OHB деңгээлинин жогорулашы HDAC ингибирлөөсүн же гистон ацетилтрансферазаны активдештирүү (Мароси ж.б., 2016; Sleiman et al., 2016) же кычкылдануу стрессине (Shimazu et al., 2013) . HDAC3 OHB бөгөт коюу жаңы төрөлгөн зат алмашуу физиологиясын жөнгө салышы мүмкүн (Rando et al., 2016). Көз карандысыз, ?OHB өзү түздөн-түз гистон лизин калдыктарын өзгөртөт (Xie et al., 2016). Узакка созулган орозо, же стептозотоцин менен шартталган диабеттик кетоацидоз гистондун ?-гидроксибутириляциясын көбөйтөт. Лизиндин ?-гидроксибутирилдениши жана ацетилденген жерлеринин саны салыштырмалуу болгонуна карабастан, ацетилденгенге караганда стехиометриялык жактан көбүрөөк гистондун ?-гидроксибутирилдениши байкалган. Айкын гендерге гистон лизининин ?-гидроксибутирилдениши, ацетилдениши же метилдениши таасир эткен, бул ар кандай клеткалык функцияларды көрсөтүп турат. ?-гидроксибутирилденүү стихиялуубу же ферменттикпи, белгисиз, бирок кетон денелери аркылуу транскрипцияга динамикалык таасир этүүчү механизмдердин спектрин кеңейтет.
Калорияны чектөө жана аш болумдуу заттардын жетишсиздиги учурундагы клетканы кайра программалоонун маанилүү окуялары SIRT3- жана SIRT5-көз каранды митохондриялык деацетилдөө жана десукцинилденүү аркылуу боор жана боордон тышкары кыртыштарда кетогендик жана кетолитикалык протеиндерди трансляциядан кийинки деңгээлде жөнгө салышы мүмкүн. 2015; Hebert et al., 2013; Rardin et al., 2013; Shimazu et al., 2010). Ээленген жерлерди стехиометриялык салыштыруу сөзсүз түрдө метаболикалык агымдын жылышына түздөн-түз байланышпаса да, митохондриялык ацетилдешүү динамикалык жана ферменттик ацетилтрансферазаларга караганда ацетил-КоА концентрациясы же митохондриялык рН менен шартталышы мүмкүн (Вагнер жана Пейн, 2013). SIRT3 жана SIRT5 кетондун денесин метаболизмдөөчү ферменттердин активдүүлүгүн модуляциялоосу ацетилпротеомду, сукцинилпротеомду жана башка динамикалык клеткалык буталарды түзүүдө кетондордун өз ара ролу жөнүндө суроону туудурат. Чынында эле, кетогенездин вариациялары NAD + концентрациясын чагылдыргандыктан, кетондун өндүрүшү жана көптүгү сиртуиндин активдүүлүгүн жөнгө салышы мүмкүн, ошону менен жалпы ацетил-КоА / сукцинил-КоА бассейндерине, ацилпротеомго жана ошону менен митохондриялык жана клетка физиологиясына таасир этет. Лизин ферментинин калдыктарынын ?-гидроксибутирилдениши уюлдук кайра программалоого дагы бир катмарды кошо алат. extrahepatic кыртыштарда, кетон дене кычкылдануу клетка гомеостазында окшош өзгөрүүлөрдү түрткү болушу мүмкүн. Ацетил-КоА бассейндерин бөлүү жогорку деңгээлде жөнгө салынган жана клеткалык өзгөрүүлөрдүн кеңири спектрин координациялаганы менен, кетон денелеринин митохондриялык жана цитоплазмалык ацетил-КоА концентрацияларын түз түзө алуу жөндөмдүүлүгү түшүндүрүүнү талап кылат (Chen et al., 2012; Corbet et al., 2016; Pougovkina et al., 2014; Schwer et al., 2009; Wellen and Thompson, 2012). Ацетил-КоА концентрациялары катуу жөнгө салынгандыктан жана ацетил-КоА мембрана өтпөгөндүктөн, ацетил-КоА гомеостазын координациялоочу механизмдерди, анын ичинде TCA циклиндеги өндүрүштүн ылдамдыгын жана терминалдык кычкылдануу ылдамдыгын, кетон денелерине айланууну, митохондриялыктарды эске алуу абдан маанилүү. карнитин ацетилтрансфераза (CrAT) аркылуу агып чыгуу, же ацетил-КоА цитратка айландырылгандан кийин цитозолго экспорттолот жана ATP цитрат-лиазасы (ACLY) менен бошотот. Клетканын ацетилпротеомундагы жана гомеостаздагы бул акыркы механизмдердин негизги ролдору кетогенездин жана кетондун кычкылдануусунун ролдорун дал түшүнүүнү талап кылат (Das et al., 2015; McDonnell et al., 2016; Moussaieff et al., 2015; Overmyer et al., 2015; Seiler et al., 2014; Seiler et al., 2015; Wellen et al., 2009; Wellen and Thompson, 2012). Метаболомикадагы жана ацилпротеомикадагы конвергенттик технологиялар, максаттарды жана натыйжаларды аныктоо үчүн генетикалык жактан башкарылган моделдердин шартында талап кылынат.
Ketone органдарына каршы жана Pro-сезгенүү Responses
Кетоз жана кетон органдары сезгенүүнү жана иммундук клетканын иштешин модуляциялайт, бирок ар түрдүү, ал тургай, карама-каршы механизмдер сунушталган. Узакка созулган аш болумдуу заттардын жетишсиздиги сезгенүүнү азайтат (Youm et al., 2015), бирок 1-типтеги кант диабетинин өнөкөт кетозу сезгенүүгө жардам берет (Jain et al., 2002; Kanikarla-Marie and Jain, 2015; Kurepa et al., 2012). ). Сезгенүүдө ?OHB үчүн механизмге негизделген сигналдык ролдор пайда болот, анткени көптөгөн иммундук системанын клеткалары, анын ичинде макрофагдар же моноциттер, GPR109A-ны мол экспрессиялайт. OHB негизинен сезгенүүгө каршы реакцияны көрсөтсө да (Fu et al., 2014; Gambhir et al., 2012; Rahman et al., 2014; Youm et al., 2015), кетон денелеринин жогорку концентрациясы, айрыкча AcAc, сезгенүүгө каршы жооп козгойт (Jain et al., 2002; Kanikarla-Marie and Jain, 2015; Kurepa et al., 2012).
GPR109A лиганддарынын атеросклероздо, семирүүдө, ичегинин сезгенүү ооруларында, нейрологиялык ооруларда жана ракта сезгенүүгө каршы ролу каралып чыкты (Graff et al., 2016). GPR109A экспрессиясы диабетик моделдердин RPE клеткаларында, адамдын диабети менен ооруган (Gambhir et al., 2012) жана микроглияда нейродегенерация учурунда көбөйөт (Fu et al., 2014). ?OHB сезгенүүгө каршы таасирлери RPE клеткаларында GPR109A ашыкча экспрессия менен күчөтүлөт жана GPR109A фармакологиялык бөгөт коюу же генетикалык нокаут менен жокко чыгарылат (Gambhir et al., 2012). OHB жана экзогендик никотин кислотасы (Taggart et al., 2005), экөө тең TNF сезгенүүгө каршы таасир берет? же сезгенүүгө каршы протеиндердин (iNOS, COX-2) же секрецияланган цитокиндердин (TNF?, IL-1?, IL-6, CCL2/MCP-1) деңгээлин төмөндөтүү жолу менен LPS менен шартталган сезгенүүнү жарым-жартылай NF ингибирлөө аркылуу -?B транслокациясы (Fu et al., 2014; Gambhir et al., 2012). ?OHB антиоксиданттык стресс реакциясын активдештирип, ER стрессин жана NLRP3 inflammasome азайтат (Bae et al., 2016; Youm et al., 2015). Бирок, нейродегенеративдик сезгенүүдө, GPR109A-каранды ?OHB-арачы коргоо MAPK жол сигнализациясы сыяктуу сезгенүү медиаторлорун камтыбайт (мисалы, ERK, JNK, p38) (Fu ж.б., 2014), бирок COX-1ге көз каранды PGD2 талап кылынышы мүмкүн. өндүрүш (Rahman et al., 2014). GPR109A макрофагынын ишемиялык инсульт моделинде нейропротектордук таасир көрсөтүү үчүн талап кылынышы кызык (Rahman et al., 2014), бирок ?OHBнин жилик чучугунан алынган макрофагдардагы NLRP3 inflammasome бөгөт коюу жөндөмдүүлүгү GPR109A көз карандысыз (Youm et al. ., 2015). Көпчүлүк изилдөөлөр ?OHB сезгенүүгө каршы таасирлери менен байланыштырса да, ?OHB сезгенүүгө каршы болушу мүмкүн жана музоо гепатоциттеринин липиддердин пероксидациясынын маркерлерин жогорулатат (Shi et al., 2014). Ошентип, ?OHB сезгенүүгө каршы таасирлери клетканын түрүнө, ?OHB концентрациясына, экспозициянын узактыгына жана ко-модуляторлордун болушуна же жоктугуна жараша болушу мүмкүн.
?OHBден айырмаланып, AcAc сезгенүүгө каршы сигналды активдештире алат. Көтөрүлгөн AcAc, өзгөчө глюкозанын жогорку концентрациясы менен, NADPH оксидазасы / кычкылдануучу стресске көз каранды механизм аркылуу эндотелий клеткасынын жаракатын күчөтөт (Kanikarla-Marie and Jain, 2015). Кант диабети менен ооруган энелердин киндигинде жогорку AcAc концентрациясы протеиндин кычкылдануу ылдамдыгы жана MCP-1 концентрациясы менен байланышта болгон (Kurepa et al., 2012). Кант диабети менен ооруган бейтаптарда жогорку AcAc TNF менен байланышта болгон? экспрессия (Jain ж.б., 2002) жана AcAc, бирок ?OHB эмес, индукцияланган TNF?, MCP-1 экспрессиясы, ROS топтолушу жана U937 адамдын моноцит клеткаларында cAMP деңгээлинин төмөндөшү (Jain et al., 2002; Kurepa et al. ., 2012).
Кетон денесине көз каранды сигнал кубулуштары көбүнчө кетон денесинин жогорку концентрациясында (> 5 мМ) гана ишке ашат жана көптөгөн изилдөөлөр кетондорду про- же сезгенүүгө каршы таасирлерге байланыштырган учурда, түшүнүксүз механизмдер аркылуу. Мындан тышкары, сезгенүү боюнча ?OHB каршы AcAc карама-каршы таасири жана AcAc/?OHB катышынын митохондриялык редокс дараметин таасир этүү жөндөмдүүлүгүнө байланыштуу, клеткалык фенотиптерге кетондук органдардын ролдорун баалоочу мыкты эксперименттер AcAc жана ? OHB ар кандай катышта жана ар кандай топтолгон концентрацияларда [мисалы, (Saito et al., 2016)]. Акыр-аягы, AcAc коммерциялык жактан литий тузу же колдонуудан мурун базалык гидролизди талап кылган этил эфири катары гана сатып алса болот. Литий катиону өз алдынча сигнал берүү каскаддарын индукциялайт (Manji et al., 1995), ал эми AcAc анион туруксуз. Акырында, рацемикалык d/l-?OHB колдонгон изилдөөлөр чаташтырылышы мүмкүн, анткени d-?OHB стереоизомери гана AcAcге кычкылданышы мүмкүн, бирок d-?OHB жана l-?OHB GPR109A аркылуу ар бир сигнал берип, NLRP3 inflammasome, жана липогендик субстрат катары кызмат кылат.
Ketone органдары, оксидаттык стресстин жана Neuroprotection
Кычкылдануу стресси, адатта, ашыкча өндүрүштүн жана/же жоюлуунун бузулушунан улам ROS ашыкча берилген мамлекет катары аныкталат. Кетон денелеринин антиоксиданттык жана кычкылдануучу стрессти басаңдатуучу ролу in vitro жана in vivo, айрыкча нейропротекциянын контекстинде кеңири сүрөттөлгөн. Көпчүлүк нейрондор май кислоталарынан жогорку энергиялуу фосфаттарды эффективдүү пайда кылбайт, бирок углеводдор жетишсиз болгондо кетон денелерин кычкылдантат, кетон денелеринин нейропротектордук таасирлери өзгөчө маанилүү (Cahill GF Jr, 2006; Edmond et al., 1987; Yang) ж.б., 1987). Кычкылдануу стресс моделдеринде, BDH1 индукциясы жана SCOT басуусу кетон денесинин метаболизмин ар түрдүү клетка сигналдарын, редокс потенциалын же метаболизмдик талаптарды колдоо үчүн кайра программаланышы мүмкүн экенин көрсөтүп турат (Nagao et al., 2016; Tieu et al., 2003).
Кетон денелери нейрондордо жана кардиомиоциттерде клеткалык зыяндын, жаракат алуунун, өлүмдүн жана төмөнкү апоптоздун деңгээлин төмөндөтөт (Haces et al., 2008; Maalouf et al., 2007; Nagao et al., 2016; Tieu et al., 2003). Чакырылган механизмдер ар түрдүү жана дайыма концентрацияга сызыктуу байланышта боло бербейт. Төмөн миллимолярдык концентрациялары (d же l)-?OHB ROS (гидроксил анион) тазалайт, ал эми AcAc көптөгөн ROS түрлөрүн тазалайт, бирок физиологиялык диапазондон ашкан концентрацияларда гана (IC50 20-67 mM) (Haces et al., 2008) . Тескерисинче, электрон ташуу чынжырынын редокс потенциалына пайдалуу таасири көбүнчө d-?OHB менен байланышкан механизм болуп саналат. Бардык үч кетон органы (d/l-?OHB жана AcAc) нейрон клеткаларынын өлүмүн жана гликолиздин химиялык бөгөт коюусунан келип чыккан ROS топтолушун азайтса, d-?OHB жана AcAc гана нейрондук ATP төмөндөшүнө жол бербейт. Тескерисинче, бир гипогликемиялык in vivo моделде, (d же l) -?OHB, бирок AcAc эмес, гиппокампалдык липиддердин пероксидациясын алдын алган (Haces et al., 2008; Maalouf et al., 2007; Marosi et al., 2016; Murphy, 2009). Tieu et al., 2003). Кетогендик диета (87% ккал май жана 13% белок) менен азыктанган чычкандардын in vivo изилдөөлөрү антиоксиданттык потенциалдын нейроанатомиялык вариациясын көрсөттү (Ziegler ж.б., 2003), мында эң терең өзгөрүүлөр гиппокампта байкалган, глутатион пероксидазасы жана жалпы саны көбөйгөн. антиоксидант касиеттери.
Кетогендик диета, кетон эфирлери (ошондой эле кетогендик диетаны жана экзогендик кетон органдарын терапевтик колдонууну караңыз), же ?OHB администрациясы ишемиялык инсульттун моделдеринде нейропротекцияны көрсөтөт (Rahman et al., 2014); Паркинсон оорусу (Tieu et al., 2003); борбордук толкунданып системасы кычкылтек уулуулугун талма (D'Agostino ж.б., 2013); эпилепсиялык спазм (Yum et al., 2015); митохондриялык энцефаломиопатия, сүт ацидоз жана инсульт сыяктуу (MELAS) эпизоддор синдрому (Frey ж.б., 2016) жана Альцгеймер оорусу (Cunnane and Crawford, 2003; Yin et al., 2016). Тескерисинче, жакында жасалган отчет митохондриялык биогенездин жана антиоксиданттык кол тамгалардын көбөйгөнүнө карабастан, анормалдуу митохондриялык ДНКны оңдоонун трансгендик чычкан моделинде кетогендик диета менен нейродегенеративдик прогрессиянын гистопатологиялык далилдерин көрсөттү (Lauritzen et al., 2016). Башка карама-каршы отчеттор жогорку кетон дене концентрациясынын таасири кычкылдануу стрессти пайда кылат деп эсептешет. Жогорку ?OHB же AcAc дозалары азот кычкылынын секрециясын, липиддердин пероксидациясын, музоо гепатоциттеринде SOD, глутатион пероксидаза жана каталаза экспрессиясынын төмөндөшүн шарттады, ал эми келемиштердин гепатоциттеринде MAPK жолунун индукциясы AcAcге таандык, бирок ?OHB (Abdelmegeed et al.2004) ; Shi et al., 2014; Shi et al., 2016).
Чогуу алганда, көпчүлүк отчеттор ?OHB кычкылдануу стрессинин басаңдашы менен байланыштырат, анткени анын администрациясы ROS/супероксиддин өндүрүшүн токтотот, липиддердин пероксидациясын жана белоктун кычкылданышын алдын алат, антиоксидант белоктун деңгээлин жогорулатат жана митохондриялык дем алууну жана ATP өндүрүшүн жакшыртат (Abdelmegeed et al., 2004; Haces ж. ж.б., 2008; Yin et al., 1998; Ziegler et al., 2002). AcAc OHBге караганда кычкылдануу стрессинин индукциясы менен түздөн-түз байланышта болгонуна карабастан, бул эффекттер дайыма эле проспективдүү сезгенүү реакцияларынан оңой ажыратыла бербейт (Jain et al., 2015; Kanikarla-Marie and Jain, 2007; Каникарла-Мари жана Джейн, 2008). Андан тышкары, плейотроптук кетогендик диеталар тарабынан берилген антиоксиданттык пайда кетон денелери тарабынан которулушу мүмкүн эмес жана кетон денелери тарабынан берилген нейропротекция толугу менен кычкылдануу стрессине байланыштуу болушу мүмкүн эмес экенин эске алуу маанилүү. Мисалы, глюкоза ажыратуу учурунда, кортикалдык нейрондордо глюкозанын ажырашынын моделинде, ?OHB autophagic агымын стимулдап, нейрондордун өлүмүнүн азайышы менен байланышкан autophagosome топтолушун алдын алган (Camberos-Luna et al., 2016). d-?OHB ошондой эле канондук антиоксидант протеиндерин FOXO2003a, SOD, MnSOD жана каталазаны HDAC ингибирлөө аркылуу индукциялайт (Nagao et al., 2016; Shimazu et al., 2003).
Келишимдик Алкоголдук Fatty Боор оорулары (NAFLD) жана Ketone Body метаболизм
Семирүү менен байланышкан NAFLD жана алкоголсуз стеатогепатит (NASH) Батыш өлкөлөрүндө боор ооруларынын эң көп кездешүүчү себептери (Rinella and Sanyal, 2016), ал эми NASH козгогон боор жетишсиздиги боорду трансплантациялоонун эң көп тараган себептеринин бири. Триацилглицериндин гепатоциттердеги ашыкча сакталышы> 5% боордун салмагы (NAFL) боордун деградациялык функциясын жаратпаса, адамдардын NAFLDге өтүшү инсулиндин туруктуулугуна жана 2-типтеги кант диабетинин көбөйүү тобокелдигине байланыштуу жана патогенезине шарт түзүшү мүмкүн жүрөк-кан тамыр оорулары жана өнөкөт бөйрөк оорулары (Fabbrini et al., 2009; Targher et al., 2010; Targher and Byrne, 2013). NAFLD жана NASH патогендик механизмдери толук түшүнүксүз, бирок гепатоцит метаболизминин бузулушун, гепатоцит аутофагиясын жана эндоплазмалык тордун стрессин, боордун иммундук клеткасынын иштешин, майлуу ткандардын сезгенүүсүн жана тутумдук сезгенүү медиаторлорун камтыйт (Фаббрини жана башкалар, 2009; Масуока жана Чаласани, 2013) ; Таргер жана башкалар., 2010; Янг жана башкалар., 2010). Углевод, липид жана аминокислота метаболизминин күчөгөндүктөрү адамдардын жана моделдик организмдердин семирүү, диабет жана NAFLDде пайда болушуна өбөлгө түзөт [Фарес жана башкалар., 2012; Лин жана Аксили, 2011; Ньюгард, 2012; Шемуел жана Шулман, 2012; Күн жана Лазар, 2013)]. Цитоплазмалык липиддик метаболизмдеги гепатоцит аномалиялары көбүнчө NAFLD (Фаббрини жана башкалар, 2010b) тарабынан байкалса, майлардын окистенип чыгарылышын жөнгө салуучу митохондриялык метаболизмдин ролу NAFLD патогенезинде анча байкалбайт. Митохондриялык метаболизмдин аномалиялары пайда болуп, NAFLD / NASH патогенезине шарт түзөт (Hyotylainen et al., 2016; Serviddio et al., 2011; Serviddio et al., 2008; Wei et al., 2008). Жалпы (Felig et al., 1974; Iozzo et al., 2010; Koliaki et al., 2015; Satapati et al., 2015; Satapati et al., 2012; Sunny et al., 2011) бар, бирок бирдей эмес ( Koliaki and Roden, 2013; Perry et al., 2016; Rector et al., 2010) ак ниеттүү NASH, боор митохондриялык кычкылдануу жана айрыкча май кычкылдануусун иштеп чыгууга чейин, семирүү, инсулиндин тутумуна туруктуулук күчөтүлөт деген консенсус. , жана NAFLD. Кыязы, NAFLD өнүккөн сайын, айрым митохондриялардын арасында да, кычкылдануу жөндөмдүүлүгүнүн гетерогендүүлүгү пайда болуп, акыры кычкылдануу функциясы начарлайт (Koliaki et al., 2015; Rector et al., 2010; Satapati et al., 2008; Satapati et al., 2012; Satapati et al.) ., XNUMX).
Кетогенез көбүнчө боордун майынын кычкылдануусу үчүн прокси катары колдонулат. Кетогенездин бузулушу жаныбарлардын моделдеринде, кыязы, адамдарда NAFLD прогресси менен пайда болот. Толук эмес аныкталган механизмдер аркылуу гиперинсулинемия кетогенезди басат, балким арык башкарууга салыштырмалуу гипокетонемияга салым кошот (Bergman et al., 2007; Bickerton et al., 2008; Satapati et al., 2012; Soeters et al., 2009; Sunny et al. , 2011; Вице ж.б., 2005). Ошого карабастан, жүгүртүүдөгү кетон денесинин концентрациясынын NAFLDди алдын ала айтуу жөндөмдүүлүгү талаштуу (M�nnist et al., 2015; Sanyal et al., 2001). Жаныбарлардын моделдериндеги бекем сандык магниттик-резонанстык спектроскопиялык методдор инсулинге орточо туруктуулук менен кетондун айлануу ылдамдыгын көрсөттү, бирок инсулинге каршылыктын төмөндөшү катуураак болгон (Satapati et al., 2012; Sunny et al., 2010). Боордун майы бар семиз адамдарда кетогендик норма нормалдуу (Бикертон ж.б., 2008; Sunny ж.б., 2011), демек, кетогенездин ылдамдыгы гепатоциттердин ичиндеги май кислотасынын жүгүн жогорулатууга салыштырмалуу азаят. Демек, ?-кычкылдануудан алынган ацетил-КоА TCA циклинде терминалдык кычкылданууга багытталышы мүмкүн, терминалдык кычкылданууну, фосфоэнолпируват менен башкарылган глюконеогенезди анаплероз/катаплероз жана кычкылдануу стресси аркылуу жогорулатат. Ацетил-КоА да митохондриядан цитрат, липогенездин прекурсордук субстраты катары экспортко кабылышы мүмкүн (4-сүрөт) (Satapati et al., 2015; Satapati et al., 2012; Solinas et al., 2015). Кетогенез инсулинге же узакка созулган семирүү менен орозо кармоого азыраак жооп берет, ал эми (Satapati ж. Акыркы далилдер mTORC2012 кетогенезди инсулин сигнализациясынын ылдый жагындагы жол менен басарын көрсөтүп турат (Кучежова ж.б., 1), бул mTORC2016 PPAR? аркылуу Hmgcs1 индукциясын тоскоол кылган байкоолорго ылайык келет (Sengupta et al., 2) ошондой эле HMGCS2010 жана SCOT/OXCT2 жобосун караңыз).

Биздин топтун алдын ала байкоолор кетогенетикалык жетишсиздигинин терс боор кесепеттерин сунуштайт (Cotter et al., 2014). Кетогенездин бузулушу, атүгүл углевод менен толукталган жана "кетогендик эмес" абалда да глюкозанын анормалдуу метаболизмине көмөктөшөт жана стеатогепатитти козгойт деген гипотезаны текшерүү үчүн биз антисенстик олигонуклеотиддерди (ASO) башкаруу аркылуу белгилүү кетогендик жетишсиздиктин чычкан моделин түздүк. Hmgcs2. Стандарттуу майы аз чою менен азыктанган чоң чычкандарда HMGCS2 жоготуусу жумшак гипергликемияга алып келип, жүздөгөн боор метаболиттеринин өндүрүшүнүн кескин көбөйүшүнө алып келди, алардын топтому липогенездин активдешүүсүн катуу сунуштады. Жетишсиз кетогенези бар чычкандарды жогорку майлуу диета менен тамактандыруу гепатоциттердин кеңири жабыркоосуна жана сезгенишине алып келди. Бул табылгалар (i) кетогенез пассивдүү толуп кетүү жолу эмес, тескерисинче боор жана интеграцияланган физиологиялык гомеостаздагы динамикалык түйүн жана (ii) NAFLD / NASH жана боор глюкозасынын бузулган метаболизмин азайтуу үчүн этият кетогендик көбөйтүүнү изилдөөгө татыктуу деген борбордук гипотезаларды колдойт. .
Бузулган кетогенез боордун жабыркашына жана глюкоза гомеостазынын өзгөрүшүнө кантип салым кошо алат? Биринчи карап чыгуу - бул күнөөлүү кетогендик агымдын жетишсиздигиби же кетондордун өздөрүбү. Жакында жасалган баяндамада кетон органдары n-3 көп тойбогон май кислоталарына жооп иретинде кычкылдануу стрессинен келип чыккан боор жаракатын азайтышы мүмкүн деп болжолдойт (Pawlak et al., 2015). Эсиңизде болсун, гепатоциттерде SCOT экспрессиясынын жоктугунан кетон денелери кычкылданбайт, бирок алар липогенезге салым кошо алат жана алардын кычкылдануусунан көз карандысыз түрдүү сигналдык ролдорду аткара алат (ошондой эле кетон денелеринин кычкылданбаган метаболикалык тагдырын жана ?OHB катары караңыз). сигнал берүүчү ортомчу). Ошондой эле гепатоциттерден алынган кетон денелери боор ацинунун ичиндеги кошуна клетка түрлөрү үчүн сигнал жана/же метаболит катары кызмат кылышы мүмкүн, анын ичинде жылдыз клеткалары жана Купфер клеткасынын макрофагдары. Колдо болгон чектелген адабияттар макрофагдардын кетон денелерин кычкылдандыра албастыгын сунуш кылганы менен, бул классикалык методологиялардын жардамы менен гана өлчөнөт жана перитонеалдык макрофагдарда гана (Newsholme et al., 1986; Newsholme et al., 1987), бул кайрадан баалоо сөөк чучугунан алынган макрофагдарда көп SCOT экспрессиясын эске алганда ылайыктуу (Youm et al., 2015).
Гепатоциттердин кетогендик агымы да цитопротектор болушу мүмкүн. Пайдалуу механизмдер кетогенезден көз каранды болбосо да, карбонгидратсыз кетогендик диеталар NAFLDдин жакшырышы менен байланышкан (Browning et al., 2011; Foster et al., 2010; Kani et al., 2014; Schugar and Crawford, 2012) . Биздин байкоолорубуз көрсөткөндөй, гепатоциттердин кетогенези TCA циклинин агымын, анаплеротикалык агымды, фосфоэнолпируваттан алынган глюконеогенезди (Cotter et al., 2014) жана ал тургай гликоген жүгүртүүнү жөнгө салышы мүмкүн. Кетогендик бузулуу ацетил-КоАны TCA агымын көбөйтүүгө багыттайт, бул боордо ROS-арачылыгы жараат көбөйүшү менен байланышкан (Satapati et al., 2015; Satapati et al., 2012); көмүртектин цитотоксиктигин далилдей турган де-ново синтезделген липиддердин түрүнө бурууга мажбурлайт; жана NADH кайра кычкылданышын алдын алат NAD + (Cotter et al., 2014) (сүрөт. 4). Биргелешип алганда, келечектеги эксперименттер салыштырмалуу кетогендик жетишсиздик адаптивдик болуп калышы мүмкүн болгон механизмдерди чечүү үчүн талап кылынат, гипергликемияга өбөлгө түзөт, стеатогепатитти козгойт жана бул механизмдер адамдын NAFLD/NASHта иштейби. Эпидемиологиялык далилдер стеатогепатиттин өрчүшү учурунда кетогенездин бузулушун көрсөтүп турат (Embade et al., 2016; Marinou et al., 2011; M�nnist� et al., 2015; Pramfalk et al., 2015; Safaei et al., 2016) боордун кетогенезин жогорулатуучу терапиялар пайдалуу болушу мүмкүн (Degirolamo et al., 2016; Honda et al., 2016).
Ketone органдары жана Heart аткарбоо (HF)
Зат алмашуу ылдамдыгы суткасына 400 ккал/кгдан ашкан жана суткасына 6-35 кг АТФ айлануусу менен жүрөк энергияны эң көп сарптаган жана кычкылдануу талабы бар орган болуп саналат (Ashrafian et al., 2007; Wang et al., 2010b). Миокарддын энергия жүгүртүүсүнүн басымдуу бөлүгү митохондрияда жашайт жана бул камсыздоонун 70% ФАОдон келип чыгат. Кадимки шарттарда жүрөк бардык жегич жана ийкемдүү, бирок патологиялык жактан кайра калыптанган жүрөк (мисалы, гипертония же миокард инфарктынан улам) жана диабетик жүрөк метаболизмдик жактан ийкемсиз болуп калат (Balasse and Fery, 1989; BING, 1954; Fukao et al., 2004). Lopaschuk et al., 2010; Taegtmeyer et al., 1980; Taegtmeyer et al., 2002; Young et al., 2002). Чынында эле, чычкан моделдеринде жүрөк күйүүчү майдын метаболизминин генетикалык программаланган аномалиялары кардиомиопатияны козгойт (Carley et al., 2014; Neubauer, 2007). Физиологиялык шарттарда кадимки жүрөк май кислотасынын жана глюкозанын кычкылданышынын эсебинен кетон денелерин алардын жеткирилишине жараша кычкылдандырат, ал эми миокард масса бирдигине эң жогорку кетон денесин керектөөчү болуп саналат (BING, 1954; Crawford et al., 2009; GARLAND et al. ., 1962; Hasselbaink et al., 2003; Jeffrey et al., 1995; Pelletier et al., 2007; Tardif et al., 2001; Yan et al., 2009). Май кислотасынын кычкылданышына салыштырмалуу кетон денелери энергиялык жактан эффективдүү болуп, жумшалган кычкылтектин бир молекуласына АТФ синтези үчүн көбүрөөк энергия берет (P/O катышы) (Kashiwaya et al., 2010; Sato et al., 1995; Veech, 2004) . Кетондун денесинин кычкылданышы да ФАОго караганда потенциалдуу жогору энергияны берет, убихинондун кычкылданышын сактайт, бул электрондорду ташуу чынжырында кычкылдануу аралыгын жогорулатат жана ATPди синтездөө үчүн көбүрөөк энергияны берет (Sato et al., 1995; Veech, 2004). Кетон денелеринин кычкылдануусу ROS өндүрүшүн, демек, кычкылдануу стрессин да азайтышы мүмкүн (Veech, 2004).
Алдын ала interventional жана байкоо жүрөгүндө ketone органдарынын болуучу пайдалуу ролун көрсөтүп турат. Сынамык Жүрөктүн ишемия оорусу / reperfusion жаракат контекстинде ketone органдары мүмкүн кардиопротектордук таасирлери (Al-Зайд, ж.б. 2007.. Wang ж.б., 2008), тетирисинче, балким, улам маанилүү кычкылданууга phosphorylation жүрөгүндө же жөнгө өсүшү митохондриялык мол медиаторлор (Snorek ж.б., 2012.. Zou ж.б., 2002). Акыркы изилдөөлөр ketone орган пайдалануу чычкандардын жүрөгүн албай жайылып баратканын көрсөтүп турат жана адамдар, анын ичинде алдын ала айткандарын колдогон адамдарга (Bing, 2016 (Обер ж.б., 2016.) (Беди, ж.б. 1954.); Fukao ж.б., 2000. Janardhan ж.б., 2011.. Longo ж.б., 2004; жалею жана Schinz, 1973; Tildon жана Cornblath, 1972). Таратылган ketone орган шогырлануы жүрөк оорусунан менен ооруган адамдар көбөйгөндө, толтуруп, кысым, байкоо, анын механизмдери жана мааниси (Kupari белгисиз бойдон калууда менен түздөн-түз байланыштуу, ж.б. 1995.. Lommi ж.б., 1996. Lommi ж.б., 1997; Neely ж.б. ., 1972), бирок, хирургиялык жол менен жасалма басым ашыкча зыян жооп cardiomyocytes Көргөзмө патологиялык карынчанын-түзөөнү жана ROS кол тездетилген ылгап Scot жетишсиздиги менен чычкандар (Schugar ж.б.., 2014).
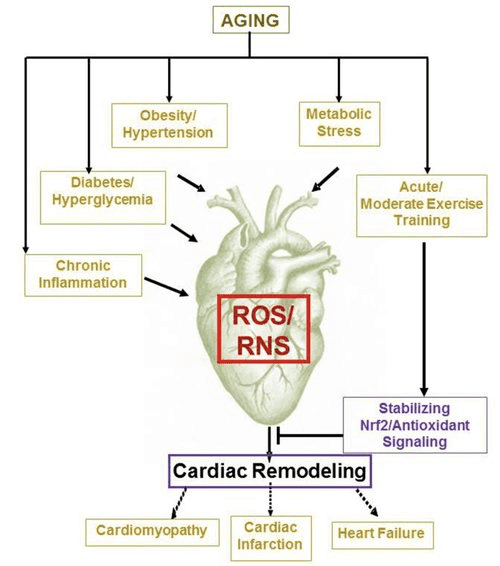
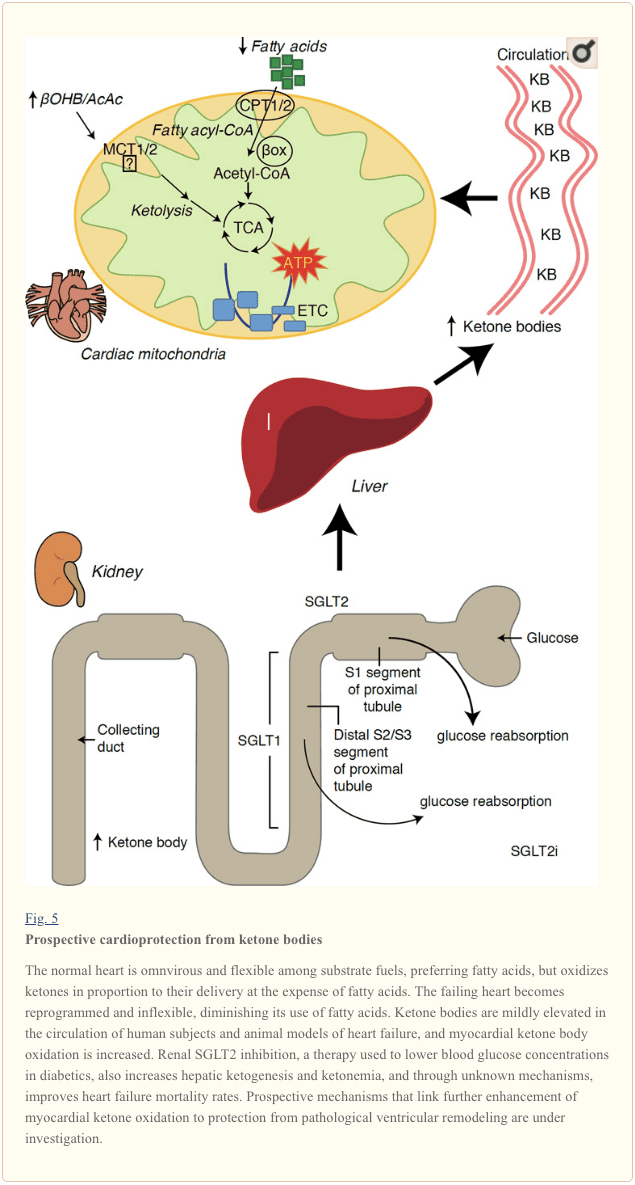
диабет терапия акыркы кызыктуу байкоолор миокарддын ketone зат жана патологиялык карынчанын каалады ортосундагы мүмкүн болгон байланышты (сүрөт. 5) ачып бердим. 2 бөйрөк proximal түтүктүү натрий / глюкоза биргелешип ташуу (SGLT2i) ажыратуу адамдардын ketone орган топтолуусу жүгүртүүдөгү көбөйөт (Ferrannini ж.б., 2016a.. Inagaki ж.б., 2015) жана чычкан (Suzuki ж.б., 2014.) Көбөйгөн аркылуу боор гликогенолиз, (Ferrannini ж.б., 2014.. Ferrannini ж.б., 2016a; Katz жана Leiter, 2015. Mudaliar ж.б., 2015). Кетчү нерсе, бул каражаттардын кеминде бир HF ооруканага кыскарган (мисалы, EMPA-ОБЛ жыйынТыК сот тарабынан ачылып берилген) жана жүрөк-кан тамыр жакшыртылган өлүмгө учуроону (Fitchett ж.б., 2016.. Sonesson ж.б., 2016; Инчуан ж.б., 2016a. ; Зинмен ж.б., 2015).. байланышкан SGLT2i пайдалуу HF жыйынтыгы артында айдоочу механизмдери жигердүү талаш бойдон калууда, ал эми аман пайда мүмкүн multifactorial эмес, келечекте анын ичинде кетоз эле эмес, салмагына пайдалуу таасирлери, кан басымы, глюкоза жана заара кислотасы баскычтарында, артериялык акыл-, сезимтал бир система, Осмос diuresis / кыскарган плазма көлөмү өсүп hematocrit (Роз жана Кан, 2016; Vallon жана Thomson, 2016). бирге, түшүнүк therapeutically HF менен ооруган же ketonemia жогорулатуу алынып, же HF иштеп чыгуу тобокелдиги өтө бийик адамдар, ал эми Клиникага чейинки жана клиникалык изилдөө жигердүү боюнча тергөө амалдары жүрүп жатат (Ferrannini ж.б. талаш бойдон калууда, 2016b.. Kolwicz, ж.б. 2016; Lopaschuk жана Verma, 2016. Mudaliar ж.б., 2016; Taegtmeyer, 2016).
Рак биология Ketone органдары
ketone органдардын жана рак ортосундагы байланыштарды тездик менен өнүгүп, ал эми мал моделдерге жана адамдар да изилдөөлөр ар кандай жыйынтыктарды берди жатышат. ketone зат динамикалуу жана аш болумдуу мамлекеттик жооп, анткени, ал, анткени так жетекчиликке алуу тамак-аш дарылоо үчүн шарттарды рак биологиялык байланыштарды умтулуу да азгыра алган жок. Рак клеткалары тездик менен клетканын таралышына кармап туруу максатында, зат reprogramming өтүүгө жана өсүштү (DeNicola жана Cantley, 2015; Паршута жана Томпсон, 2016). классикалык Warburg рак клеткасы зат гликолиз жана сүт кислотасы ачытуучу кожоюндук ролуна энергиясын жана кычкылданууга phosphorylation боюнча көз карандылыкты азайтуу үчүн ордун толтурууга, ошондой эле чектелген митохондриялык дем алуу (де-өткөрүп берүү туулат таасир Feyter ж.б., 2016. Grabacka ж.б., 2016. . Канг, ж.б. 2015. Poff ж.б., 2014; Shukla ж.б., 2014).. Глюкоза көмүртек, негизинен, гликолиз аркылуу багытталган, Кребстин кездешүүчү жолуна жана lipogenesis, чогуу шишик биомассанын өсүшү үчүн зарыл болгон арачылардын камсыз кылуу (Grabacka .Удаалаш, 2016.. Shukla ж.б., 2014; Yoshii ж.б., 2015.). ажыратууга глюкозага рак клеткалары кайра жасоо, анын ичинде эжеке, глутамин, жана аспартат күйүүчү май булактарын пайдаланууга жөндөмдүү аркылуу пайда болот (Jaworski ж.б., 2016. Sullivan, ж.б. 2015.). Мисалы, кайра карату чектөөгө мүмкүндүк энергетики и анаболикалык муктаждыктарын да сактоо, carboxylation менен acetyl-КоА салып глутамин динине рагы клеткаларынын жөндөмүн ачып берет (Янг и др., 2014). рак клеткаларынын бир кызык ылайыкташуу бир күйүүчү май катары эжеке колдонуу болуп саналат (Comerford ж.б., 2014.. Jaworski ж.б., 2016. Mashimo .Удаалаш, 2014; Райт жана Симона, 2016; Yoshii ж.б., 2015.). Эжеке, ошондой эле шишик клетка жайылтпоо үчүн маанилүү lipogenesis үчүн субстрат болуп саналат, ал эми бул lipogenic түтүгүнүн пайда кыска сабыр жашоо жана көбүрөөк шишик жүк (Comerford ж.б. менен байланышкан, 2014.. Mashimo .Удаалаш, 2014; Yoshii ж.б. ., 2015).
Рак эмес клеткалар глюкозанын жетишсиздиги учурунда энергия булагын глюкозадан кетон денелерине оңой жылдырат. Бул пластикалык рак клеткаларынын түрлөрү арасында өзгөрүлмө болушу мүмкүн, бирок in vivo имплантацияланган мээ шишиги кычкылданат [2,4-13C2] -?OHB курчап турган мээ кыртышы сыяктуу даражада (De Feyter et al., 2016). "Тескери Варбург эффектиси" же "эки бөлүмдүү шишик метаболизми" моделдери рак клеткалары чектеш фибробласттарда OHB өндүрүшүн индукциялап, шишик клеткасынын энергия муктаждыгын камсыздайт (Bonucelli et al., 2010; Martinez-Outschoorn et al., 2012) . Боордо, гепатоциттердин кетогенезден кетон кычкылданышына гепатоцеллюлярдык рак (гепатома) клеткаларында жылышы эки гепатома клетка линияларында байкалган BDH1 жана SCOT иш-аракеттеринин активдешүүсүнө шайкеш келет (Чжан ж.б., 1989). Чынында эле, гепатома клеткалары OXCT1 жана BDH1ди билдирип, кетондорду кычкылдандырат, бирок сыворотканы ачка калганда гана (Huang et al., 2016). Же болбосо, шишик клеткасынын кетогенези да сунушталган. Кетогендик ген экспрессиясынын динамикалык жылыштары жоон ичеги эпителийинин рактык трансформациясы учурунда көрсөтүлөт, адатта HMGCS2ди туюндурган клетканын түрү жана акыркы отчетто HMGCS2 колоректалдык жана сквамо клеткалуу рактын начар прогнозунун прогностикалык маркери болушу мүмкүн деп болжолдонот (Камареро жана башкалар. 2006; Чен ж.б., 2016). Бул бирикме кетогенезди талап кылабы же камтыйбы, же HMGCS2нин ай жарыгы функциясы аныктала элек. Тескерисинче, PPAR тарабынан стимулданган меланома жана глиобластома клеткалары тарабынан ачык ?OHB өндүрүшү? агонист fenofibrate, өсүү камакка алуу менен байланышкан (Grabacka ж.б., 2016). Рак клеткаларында HMGCS2/SCOT экспрессиясынын, кетогенездин жана кетондун кычкылданышынын ролун мүнөздөш үчүн кошумча изилдөөлөр талап кылынат.
Күйүүчү майдын метаболизминин чөйрөсүнөн тышкары, кетондор жакында рак клеткасынын биологиясына сигнал берүү механизми аркылуу тартылган. BRAF-V600E+ меланомасынын анализи HMGCLдин OCT1ге көз каранды индукциясын онкогендик BRAFга көз каранды түрдө көрсөттү (Канг ж.б., 2015). HMGCL көбөйүшү уюлдук AcAc концентрациясынын жогору болушу менен байланыштырылды, бул өз кезегинде BRAFV600E-MEK1 өз ара аракеттенүүсүн күчөтүп, шишик клеткаларынын көбөйүшүн жана өсүшүн шарттаган MEK-ERK сигналын алдыга илгерилетти. Бул байкоолор бир сигнал механизмин колдойт келечектүү extrahepatic кетогенез кызыктуу суроону көтөрөт (ошондой эле карагыла? Ошондой эле AcAc, d-?OHB жана l-?OHB рактын метаболизмине көз карандысыз таасирин эске алуу маанилүү жана HMGCL эске алганда, лейцин катаболизми да бузулушу мүмкүн.
Рак жаныбарларынын моделдеринде кетогендик диетанын таасири (ошондой эле кетогендик диетаны жана экзогендик кетон денелерин терапевтик колдонууну караңыз) ар түрдүү (De Feyter et al., 2016; Klement et al., 2016; Meidenbauer et al., 2015; Poff et al. ., 2014; Seyfried et al., 2011; Shukla et al., 2014). Семирүү, рак жана кетогендик диеталар арасындагы эпидемиологиялык ассоциациялар талкууланып жатканда (Liskiewicz et al., 2016; Wright and Simone, 2016), жаныбарлардын моделдеринде жана адамдардын изилдөөлөрүндө кетогендик диетаны колдонуу менен мета-анализ жашоого жакшы таасирин тийгизген. Кетоздун чоңдугуна, диетаны баштоо убактысына жана шишиктин жайгашкан жерине байланыштуу пайдалар (Klement et al., 2016; Woolf et al., 2016). Кетон денелери (d-?OHB же AcAc) менен уйку безинин рак клеткаларын дарылоо өсүүнү, пролиферацияны жана гликолизди, ал эми кетогендик диетаны (81% ккал май, 18% белок, 1% углевод) in vivo шишиктин салмагын, гликемияны жана имплантацияланган рак менен ооруган жаныбарларда булчуңдардын жана дене салмагынын көбөйүшү (Shukla et al., 2014). Окшош натыйжалар диетада кетон кошумчасын алган чычкандардын метастатикалык глиобластома клеткасынын моделин колдонуу менен байкалган (Poff et al., 2014). Тескерисинче, кетогендик диета (91% ккал май, 9% белок) айлануудагы OHB концентрациясын көбөйтүп, гликемияны азайтты, бирок глиомалуу келемиштерде шишиктин көлөмүнө же жашоо узактыгына эч кандай таасир тийгизген эмес (De Feyter et al., 2016). Глюкозанын кетон индекси адамдарда жана чычкандарда кетогендик диетадан келип чыккан мээ рагын дарылоонун метаболизмин жакшыртуучу клиникалык көрсөткүч катары сунушталган (Meidenbauer et al., 2015). Бирге алганда, кетон денесинин метаболизминин жана кетон денелеринин рак биологиясындагы ролу укмуштуудай болуп саналат, анткени алардын ар бири дарылоонун натыйжалуу варианттарын түзөт, бирок негизги аспектилери өзгөрүлмөлөрдүн матрицасынан келип чыккан ачык таасирлер менен, анын ичинде (i) экзогендик кетондун ортосундагы айырмачылыктар менен түшүндүрүлөт. организмдер кетогендик диетага каршы, (ii) рак клеткасынын түрү, геномдук полиморфизмдер, даражасы жана баскычы; жана (iii) кетотикалык абалга кабылуу убактысы жана узактыгы.

Гликогенолиз, май кислоталарынын жана кетогенетикалык амино-кислотадан ажырашынан аркылуу ketone органдары тарабынан түзүлөт. Бул биохимиялык кайра кан глюкоза бир жоктугу үчүн жооп катары орозо шартта, ар кандай органдар, атап айтканда мээнин энергия менен камсыз кылат. Ketone органдар, негизинен боор клеткаларынын митохондрия өндүрүлөт. башка клеткалар гликогенолиз, ишке ашыра ала турган болсо, алар боор клеткалары катары кылып карата абал боюнча күчүнө кире элек. гликогенолиз, митохондрия болот, анткени, анын жараяндар өз алдынча жөнгө салынат. Dr. Алекс Хименес DC, демекчи Insight
Кетогенетикалык диета жана Тышкы Ketone органдарынын дарылоо Application
Кетогендик диеталардын жана кетон денелеринин терапиялык каражаттар катары колдонулушу семирүү жана NAFLD / NASH сыяктуу рак эмес контексттерде пайда болгон (Browning et al., 2011; Foster et al., 2010; Schugar and Crawford, 2012); жүрөк жетишсиздиги (Huynh, 2016; Kolwicz et al., 2016; Taegtmeyer, 2016); нейрологиялык жана нейродегенеративдик оору (Мартин ж.б., 2016; McNally жана Hartman, 2012; Rho, 2015; Rogawski ж.б., 2016; Янг жана Ченг, 2010; Yao ж.б., 2011); зат алмашуунун тубаса каталары (Scholl-B�rgi et al, 2015); жана көнүгүү аткаруу (Cox et al., 2016). Кетогендик диетанын эффективдүүлүгү эпилепсиялык талмаларды дарылоодо, өзгөчө, дары-дармекке туруктуу бейтаптарда өзгөчө бааланган. Көпчүлүк изилдөөлөр педиатриялык бейтаптардагы кетогендик диетаны баалашты жана 50 айдан кийин талма жыштыгынын ~ 3% га чейин кыскарышын, тандалган синдромдордо эффективдүүлүгүн жогорулатты (Wu et al., 2016b). Чоң кишилердин эпилепсиясында тажрыйба көбүрөөк чектелген, бирок ушундай эле кыскаруу симптоматикалык жалпыланган эпилепсия менен ооруган бейтаптарда жакшыраак жооп берүү менен байкалат (Nei et al., 2014). Негизги антиконвульсант механизмдери түшүнүксүз бойдон калууда, бирок болжолдонгон гипотезаларга глюкозаны пайдалануу/гликолиз, кайра программаланган глутамат ташуу, ATP сезгич калий каналына же аденозин A1 рецепторуна кыйыр таасир, натрий каналынын изоформасынын экспрессиясынын өзгөрүшү же айлануучу гормондорго таасирлери кирет. Lambrechts et al., 2016; Lin et al., 2017; Lutas and Yellen, 2013). Анти-конвульсант таасири, биринчи кезекте, кетон денелеринен же карбонгидратсыз диетанын каскаддык метаболизмдик кесепеттеринен уламбы, белгисиз бойдон калууда. Ошого карабастан, кетон эфирлери (төмөндө караңыз) провокацияланган талмалардын жаныбарлар моделдеринде талма босогосун көтөрөт (Ciarlone et al., 2016; D'Agostino et al., 2013; Viggiano et al., 2015).
Чок-стили жана кетогенетикалык төмөн карбонгидрат диетанын көп жагымсыз болуп эсептелет, ал эми ич катууга, hyperuricemia, hypocalcemia, hypomagnesemia, nephrolithiasis жетекчиликти колго, ketoacidosis, hyperglycemia жана холестерин жана эркин май кислотасы топтолуусу жүгүртүүдөгү жогорулатуу (Bisschop алып .Удаалаш алып келиши мүмкүн., 2001 ; Kossoff жана Хартман, 2012. Kwiterovich ж.б., 2003; Suzuki ж.б., 2002).. Ушул себептен улам, узак мөөнөттүү сактоо көйгөйлөрдү жаратууда. Грызун изилдөөлөр, адатта, бекем кетоз эткендей айырмалоочу macronutrient бөлүштүрүү (94% ккал майын, 1% ккал карбонгидрат, 5% ккал белок, Bio-Serv F3666) колдонуу. Бирок, белок мазмунду кетоз да 10% ккал кыйла менен жокко чыгарат, ошондой эле 5% ккал белок чектөө адаштырышты метаболизмдик жана психологиялык кесепеттерин ыйгарат жогорулатуу. Бул диета, иштеп чыгуу, ошондой эле холин түгөнгөндө, боор зыян чалдыгуу таасир башка бир өзгөрмө, ал тургай, гликогенолиз, (Garbow ж.б., 2011 жатат. Jornayvaz ж.б., 2010. Кеннеди, ж.б. 2007. Pissios ж.б., 2013. Schugar .Удаалаш., 2013). чычкандардын кетогенетикалык азыктанган узак мөөнөттүү керектөөнүн Effects толук аныкталган, ал эми алтын чычкандардын акыркы изилдөөлөр өз өмүрүндө үстүнөн кетогенетикалык азыктанган боюнча чычкандар, боорго зыян маркерлер нормалдуу аман жана жок экени, амино-кислота зат да, энергия жумшалуусу жана инсулин сигналдаштыруунун бойдон кыйла келёсймй (Douris .Удаалаш., 2015) алынган.
ундарды кетогенетикалык механизмдерин жакынсызбы аркылуу кетоз жогорулатуу механизмдери ingestible ketone орган прекурсорлорду пайдаланууну камтыйт. экзогендик ketone органдарынын башкаруу клеткалар глюкоза ээлөө жана пайдалануу аябайт болушу мүмкүн, ал эми, глюкоза жана инсулин шогырлануы жүгүртүүдөгү салыштырмалуу нормалдуу, анткени нормалдуу дене менен жолуккан эмес, өзгөчө психологиялык абалын жаратышы мүмкүн. Кетон денелеринин жарым ажыроо мезгили кыска, жана терапиялык кетозго жетишүү үчүн натрий ?OHB тузун жутуу же инфузиялоо натрийдин жагымсыз жүгүн козгойт. R/S-1,3-бутандиол – бул уулуу эмес диалкогол, ал боордо оңой кычкылданат, d/l-?OHB (Desrochers et al., 1992). Ар кандай эксперименталдык контексттерде бул доза чычкандарга же келемиштерге жети жумага чейин күн сайын берилип, 5 сааттын ичинде 2 мМ чейин айлануучу OHB концентрациясын түздү, ал жок дегенде кошумча 3 саатка (D') туруктуу болот. Agostino et al., 2013). тамак-жарым-жартылай бөгөт R / S-1,3-butanediol (Карпентер жана Гроссман, 1983) берилген кемирүүчүлөрдүн байкалган. Мындан тышкары, үч химиялык айырмаланган кетон эфирлери (KEs), (i) R-1,3-butanediol жана d-?OHB моноэфири (R-3-hydroxybutyl R-?OHB); (ii) глицерин-трис-?OHB; жана (iii) R,S-1,3-butanediol acetoacetate диэстери, ошондой эле кеңири изилденген (Brunengraber, 1997; Clarke et al., 2012a; Clarke et al., 2012b; Desrochers et al., 1995a Desrochers et al.; ., 1995b; Kashiwaya et al., 2010). Биринчинин мүнөздүү артыкчылыгы ичегиде же боордо эстеразанын гидролизинен кийин бир моль КЭге 2 моль физиологиялык d-?OHB түзүлөт. Коопсуздук, фармакокинетика жана толеранттуулук R-3-гидроксибутил R-?OHB-ны 714 мг/кг чейинки дозаларда жуткан адамдарда кеңири изилденген, ал эми циркуляциядагы d-?OHB концентрациясын 6 мМге чейин берген (Clarke et al., 2012a; Cox et al., 2016; Kemper et al., 2015; Shivva et al., 2016). кемирүүчүлөрдүн, бул KE калориялуу алууну жана плазманы жалпы холестеролду төмөндөйт, күрөң кемик түрткү берип, инсулин каршылыгына жакшыртат (Kashiwaya .Удаалаш, 2010.. Kemper, ж.б. 2015; Veech, 2013). Акыркы табылгалар машыгуу учурунда R-3-гидроксибутил R-?OHB жутуу скелет булчуңдарынын гликолизинин жана плазмадагы лактат концентрациясынын азайгандыгын, триацилглицеролдун булчуңга кычкылданышын көбөйтүп, карбонгидрат инсулин секрециясын биргелешип жутканда да булчуңдардын гликогенин сактап калганын көрсөтүп турат. Кокс ж.б., 2016). туруктуу көнүгүү аткарууда жакшыртуу басымдуу 2 / 8 сабактар боюнча KE үчүн бекем жооп менен шартталган, анткени бул кызыктуу жыйынтыктарды андан ары өнүктүрүү, талап кылынат. Ошентсе да, бул натыйжалар башка уланган ашуун ketone кычкылданууга үчүн артыкчылык көрсөтүп классикалык изилдөөлөрдү колдоо керек (Garland .Удаалаш, 1962. Хасселбайнк ж.б., 2003. Stanley, ж.б. 2003.. Valente-Silva .Удаалаш, 2015), анын ичинде, машыгуу учурунда, ошондой эле даярдалган спортчулар дагы башыма кетондорго пайдалануу болушу мүмкүн (Джонсон, ж.б. 1969a. Джонсон жана Уолтон, 1972. Winder ж.б., 1974. Winder ж.б., 1975). Акыр-аягы, механизмдер бирдей калориялуу алууда төмөнкү жакшыртылган көнүгүү аткарууну колдойт мүмкүн (differentially МАКРОАЗЫКТАРДЫН арасында бөлүштүрүлгөн) жана бирдей кычкылтек жеке керектөөнүн өсүш темпинин аныкталат бойдон калууда.
Future көз
Карбонгидрат чектелген мамлекеттерде майдын күйүүсүнөн чыккан уулуу заттардын бөлүнүп чыгуучу жолу катары стигматизацияланган соң (кетотоксик парадигмасы), акыркы байкоолор кетондун организминин метаболизми карбонгидраттуу шарттарда да пайдалуу роль ойнойт деген түшүнүктү колдойт. � гипотеза. Кетондун метаболизмин башкаруу үчүн жеңил тамактануу жана фармакологиялык ыкмалар аны жагымдуу терапевтикалык максатка айландырса да, агрессивдүү түрдө коюлган, бирок этият эксперименттер базалык жана котормо изилдөө лабораторияларында калууда. Жүрөк жетишсиздиги, семирүү, NAFLD/NASH, 2-типтеги диабет жана рак ооруларында кетон метаболизминин ролун аныктоодо канааттандырылбаган муктаждыктар пайда болду. Кетон денелеринин "канондук эмес" сигналдык ролдорунун масштабы жана таасири, анын ичинде метаболизм жана сигналдык жолдорго артка жана алдыга багыт берүүчү PTMлерди жөнгө салуу тереңирээк изилдөөнү талап кылат. Акыр-аягы, боордон тышкаркы кетогенез кызыктуу паракриндик жана автокриндик сигнал механизмдерин жана нерв системасындагы жана шишиктердеги метаболизмге таасир этүү мүмкүнчүлүктөрүн ачып, терапиялык максаттарга жетиши мүмкүн.
Acknowledgments
Ncbi.nlm.nih.gov/pmc/articles/PMC5313038/
Шилтемелер
Жыйынтыктап айтканда, кетон денелери адамдын денесинде жеткиликтүү глюкоза жетишсиз болгондо энергия булагы катары колдонуу үчүн боор тарабынан түзүлөт. Кетогенез кандагы глюкозанын деңгээли төмөн болгондо, айрыкча башка клеткалык углеводдор запасы түгөнгөндөн кийин пайда болот. Жогорудагы макаланын максаты кетон денелеринин күйүүчү майдын метаболизминде, сигнализациясында жана терапиясында көп өлчөмдүү ролун талкуулоо болгон. Биздин маалыматтын көлөмү хиропрактика жана омуртка ден соолук маселелери менен гана чектелет. Теманы талкуулоо үчүн доктор Хименеске кайрылыңыз же биз менен байланышыңыз915-850-0900 .
Dr. Alex Хименес менен тандалган
Шилтеме келтирилген: Ncbi.nlm.nih.gov/pmc/articles/PMC5313038/

Кошумча Тема боюнча Талкуу: Белдин Кескин Оору
Бел оорусуOf дүйнө жүзү боюнча майыптыктын жана жумушка чыкпай калган күндөрдүн эң көп кездешкен себептеринин бири. Белдин оорушу жогорку респиратордук инфекциялардан көп болгон дарыгерлердин кеңсесине баруунун экинчи жалпы себеби болуп саналат. Калктын болжол менен 80 пайызы өмүр бою жок дегенде бир жолу белдин оорушун сезишет. Омуртка - бул башка жумшак ткандардын катарында сөөктөрдөн, муундардан, байламталардан жана булчуңдардан турган татаал түзүлүш. Жаракат алуу жана / же оорлотулган шарттар, мисалы herniated дисктерде, акыры белдин оорушун белгилерине алып келиши мүмкүн. Спорттук жаракат же жол кырсыгынан жаракат алган учурлар көбүнчө белдин оорушун шарттайт, бирок кээде жөнөкөй кыймылдар оор натыйжаларга алып келиши мүмкүн. Бактыга жараша, хиропрактикага кам көрүү сыяктуу дарылоонун альтернативдүү жолдору, омуртка тууралоолорун жана кол менен иштөөнү колдонуп, белдин оорушун басаңдатып, акыры ооруну басаңдатууну жакшыртууга жардам берет.

EXTRA EXTRA | МААНИЛҮҮ ТЕМА: сунушталууда El Paso, TX Хиропрактик
***